Onco-thoracique
Cancer bronchique NPC : évolution de la place des inhibiteurs de ALK après l’ESMO 2021
Les inhibiteurs de ALK sont parfaitement légitimes en 1ère ligne métastatique mais leur ordre d’utilisation n’est pas encore pleinement défini après l’ESMO 2021. A l’avenir, ils seront probablement utilisés à des stades plus précoces.
- Rasi Bhadramani/istock
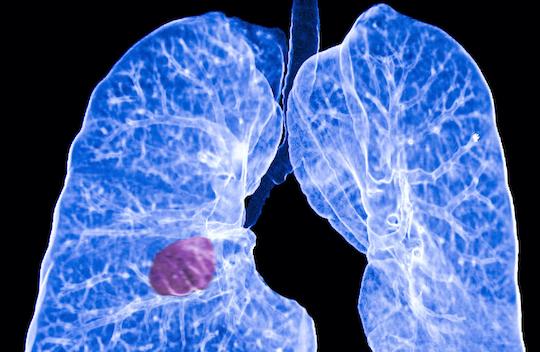
Les inhibiteurs de ALK sont utilisés aujourd’hui en première ligne métastatique du cancer bronchique non à petites cellules avec réarrangement de ALK. Cette altération moléculaire est retrouvée dans environ 8% des adénocarcinomes.
Les avancées de l'ESMO 2021
L’alectinib (600 mg x 2/j) a démontré une efficacité supérieure au crizotinib (250mg x 2/j) en première ligne métastatique avec un meilleur taux de survie sans événement à 12 mois de 68,4% versus 48,7% et un HR pour décès ou progression à 0,47 (IC à 95% : 0.34-0.65 ; p<0.001). Son efficacité est particulièrement notable dans le contrôle des métastases cérébrales connues, ou dans le délai d’apparition de métastases cérébrales2.
L’étude ALTA-1L a comparé le brigatinib (90 mg x1/j pendant 7j puis 180 mg x1/j) au crizotinib (250 mg x2/j)3. Le HR pour la survie sans progression est de 0,49 (IC à 95% : 0.33-0.74 ; p<0,001) avec un possible bénéfice pour les métastases cérébrales et les mutation p53 associées.
Le lorlatinib, TKI anti-ALK de troisième génération, a été comparé en première ligne au crizotinib dans l’étude de phase III CROWN4. L’analyse intermédiaire montre une survie sans progression médiane de 9,3 mois avec le crizotinib alors qu’elle n’est pas atteinte avec le lorlatinib (HR=0.28 ; IC à 95 % : 0.19-0.41). Le lorlatinib n’a pas d’AMM en première ligne en France ni en Europe. Les données présentées à l’ESMO 2021 rapportent dans l’essai CROWN un taux de survie sans progression à 12 mois de 78% (IC à 95% : 70-84) dans le groupe lorlatinib versus 39% (IC à 95% : 30-48) dans le groupe crizotinib. Le HR du délai de survenue de progression intra-crânienne est de 0,07 (ICà 95% : 0.03-0.17) en faveur du bras lorlatinib.
Une stratégie thérapeutique pas encore pleinement définie
Cependant, si l’utilisation d‘un TKI anti-ALK en première intention est une stratégie thérapeutique validée au stade métastatique, la question reste de savoir dans quel ordre ces molécules doivent être utilisées au cours de l’évolution de la maladie.
Des données récentes rapportent en effet que l’activation de MET est un des principaux mécanismes de résistance acquis par la tumeur sous lorlatinib. Lorsque le lorlatinib est utilisé en 3ème ligne (après crizotinib puis TKI de 2ème génération), le taux de survenue d’activation de MET est inférieur à 25%. En revanche ce taux approche les 50% lorsque le lorlatinib est utilisé en 2ème ligne après un TKI de 2ème génération5.
Le TPX-0131 est un TKI anti-ALK de 4ème génération, à large spectre, ayant une action sur les mécanismes de résistance connus. Cette drogue est actuellement en cours de développement dans un essai de phase 1/26.
Les inhibiteurs de ALK seront probablement à l’avenir utilisés aux stades plus précoces
L’essai de phase III E4512-ALCHEMIST propose du crizotinib versus abstention thérapeutique en adjuvant (patient opéré jusqu’au stade IIIA avec réarrangement de ALK) ; et l’essai ALINA (BO40336)8 propose en adjuvant de l’alectinib versus 4 cycles de chimiothérapie à base de platine chez les patients opérés d’un CBNPC réarrangé ALK (jusqu’au stade IIIA).
Les inhibiteurs de ALK ont pris leur place en 1ère ligne métastatique du CBNPC réarrangé ALK, mais la séquence d’utilisation des différentes molécules disponibles n’est pas encore clairement établie du fait de l’apparition de mécanismes de résistance.
Les TKI anti-ALK de 4ème génération, actuellement en développement, apporteront peut-être une réponse à cette problématique. Par ailleurs la prescription des inhibiteurs de ALK va probablement s’élargir dans les années à venir aux tumeurs localisées opérées en situation adjuvante.
Bibliographie
1Table ronde ESMO 2021, Ibiayi Dagogo-Jack, Todd M. Bauer, Nicolas Girard, Benjamin Solomon
2 Peters S, Camidge DR, Shaw AT, Gadgeel S, Ahn JS, Kim D-W, et al. Alectinib versus Crizotinib in Untreated ALK-Positive Non-SmallCell Lung Cancer. N Engl J Med. 31 2017;377(9):829‑38
3 Camidge DR, Kim HR, Ahn M-J, Yang JC-H, Han J-Y, Lee J-S, et al. Brigatinib versus Crizotinib in ALK -Positive Non–Small-Cell Lung Cancer. N Engl J Med. 22 nov 2018;379(21):2027‑39.
4 Shaw AT, Bauer TM, de Marinis F, Felip E, Goto Y, Liu G, et al. First-Line Lorlatinib or Crizotinib in Advanced ALK -Positive Lung Cancer. N Engl J Med. 19 nov 2020;383(21):2018‑29.
5 Dagogo Jack I, et al. Clin Cancer Res 2020; 26:2525-2545
6 Murray BW, et al. Mol Cancer Ther 2021;20:1-9