Rhumatologie
Polyarthrite rhumatoïde : les auto-anticorps du liquide synovial sont impliqués dans la destruction articulaire
Une nouvelle étude montre que, dans le liquide articulaire de la polyarthrite rhumatoïde, il n’existe pas un anticorps particulier, mais plutôt un mélange d’anticorps qui serait le principal facteur responsable de la sévérité de l’inflammation et des lésions articulaires.
- Tharakorn/istock
Selon une nouvelle technique capable d’isoler différents types d’anticorps dans différents types de liquides, une équipe suédoise a été à même d’analyser les 19 types d’ACPA (anticorps anti-protéine citrullinée) dirigés contre différents fragments de protéines contenant de la citrulline (fillagrine, α-enolase, vimentin, collagen type II, fibrinogen and histones) dans le sérum et le liquide synovial de 77 malades souffrant de polyarthrite rhumatoïde.
Aucun ACPA, pris isolément, n’a été associé plus qu’un autre à l’intensité de l’inflammation ou des lésions articulaires. Le taux d’auto-anticorps dans le liquide synovial est plus bas que dans le sérum et n’est pas corrélé à la sévérité de la maladie articulaire. Il s’agit plutôt d’un mélange de différents ACPA qui est retrouvé dans les complexes immuns du liquide synovial (« polyclonalité ») et c’est ce mélange qui est associé à différents degrés d’inflammation et de lésions articulaires. Cette étude est parue dans Annals of the Rheumatic Diseases.
PR : une maladie hétérogène
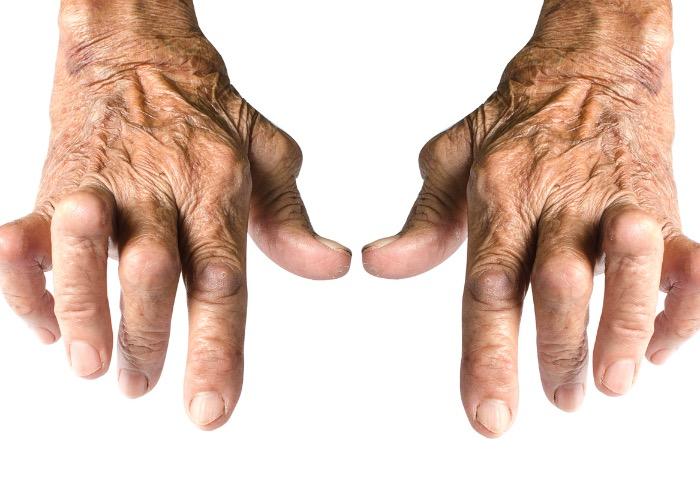
La polyarthrite rhumatoïde est une maladie inflammatoire chronique d’origine auto-immune qui s’accompagne chez environ deux tiers des malades d’anticorps anti-protéine citrullinée (anti-CCP ou ACPA). Ces ACPA simplifient le diagnostic quand ils sont présents, mais ils ont également un rôle pronostique puisqu’ils sont plus souvent associés à une inflammation plus intense, à une évolution plus sévère et à des destructions articulaires plus fréquentes.
La recherche a démontré des différences génétiques entre les malades qui ont des ACPA et ceux qui n’en n’ont pas. L’apparition d’une PR avec anticorps anti-CCP est également fortement associée au tabagisme, ce qui n’est pas le cas chez les PR qui n’ont pas d’ACPA. Ainsi les polyarthrites rhumatoïdes avec ou sans ACPA représentent 2 maladies inflammatoires articulaires différentes mais qui commencent avec un tableau clinique identique.
Une nouvelle technique d'analyse des ACPA
La plupart des tests immunologiques sont capables de détecter les ACPA indépendamment du type de la protéine avec laquelle ils réagissent, mais il est connu que différentes polyarthrites rhumatoïdes avec ACPA ont des anticorps qui ciblent différents types de protéines ou de fragments de protéines citrullinées.
Quand ces anticorps rencontrent un de ces fragments de protéines qu’ils ciblent in vitro, ils forment des complexes immuns. Des complexes immuns avaient été isolés dans le liquide articulaire de PR il y a plusieurs années, mais avec des disparités selon les études. De plus, il n’avait pas été réellement possible jusqu’à présent de démontrer que ces complexes immuns étaient capables de se former avec les ACPA dans l’articulation pour y causer une inflammation. Surtout, il n’avait pas été possible de savoir quels types d’ACPA étaient à l’origine de l’inflammation.
Un mélange d’ACPA à l’origine de l’inflammation articulaire
Avec cette nouvelle méthode, l’équipe suédoise a été à même de montrer que, dans la polyarthrite rhumatoïde avec ACPA, ces anticorps peuvent avoir un rôle pathogène direct en formant des complexes immuns à l’intérieur de l’articulation, ce qui déclenche une inflammation. Aucun ACPA en particulier ne semble responsable de cette inflammation. Au contraire, c’est un large éventail d’ACPA dans les complexes immuns articulaires qui est responsable de l’inflammation synoviale et du processus de destruction articulaire. C’est la variété plus que le taux d’ACPA qui est corrélé à l’inflammation (« polyclonalité »).
Ces résultats sont cohérents avec les modèles animaux d’arthrites auto-immunes qui montraient déjà que différents types d’auto-anticorps pour la même protéine étaient nécessaires simultanément pour provoquer une inflammation. La reproduction de cette technique sur des groupes plus important de malades pourrait permettre d’identifier les profils d’ACPA les plus à risque de destruction articulaire.