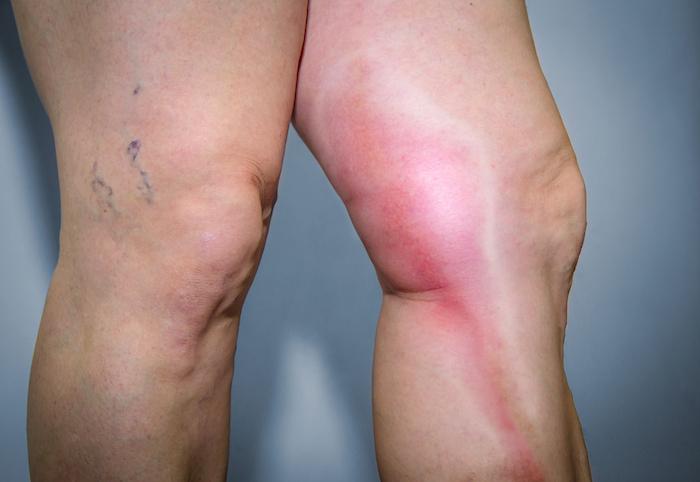
Oncologie
Cancer et thrombose : prolonger l’anticoagulation en prévention sans risque hémorragique
Dans les cancers à risque de thrombose, après 6 mois d’anticoagulation initiale, la dose réduite d’un AOD, l’apixaban, prévient les thromboses récidivantes avec un moindre risque hémorragique.
- iLexx/istock
La prise en charge de la maladie thromboembolique veineuse (MTEV) chez les patients atteints de cancer représente un défi clinique, car ces patients ont à la fois un risque accru de thrombose récidivante et de complications hémorragiques. Il y a 20 ans, l’essai CLOT a montré l'efficacité supérieure de la daltéparine par rapport aux antagonistes de la vitamine K dans la prévention des thromboses veineuses récidivantes chez les patients atteints de cancer et a établi un traitement de 6 mois d'héparine de bas poids moléculaire en tant que traitement standard des thromboses associées au cancer. Actuellement, les recommandations préconisent de prolonger l’anticoagulation tant que le cancer reste actif, sans pour autant définir clairement le schéma optimal après les 6 premiers mois.
L’essai randomisé API-CAT a évalué si une dose réduite d’apixaban (2,5 mg deux fois par jour) était non-inférieure à la dose complète (5 mg deux fois par jour) pour prévenir les récidives de MTEV chez 1766 patients avec cancer actif ayant déjà complété au moins 6 mois d’anticoagulation initiale. Après 12 mois de suivi, la dose réduite s’est révélée non-inférieure à la dose complète en termes de récidives thromboemboliques (incidence cumulée 2,1 % vs 2,8 %, HR ajusté 0,76 ; IC à 95 % : 0,41-1,41 ; p<0,001 pour non-infériorité). Les résultats de l’étude ont été présentés un congrès annuel de l’American College of Cardiology et publiés dans le New England Journal of Medicine.
Réduction des hémorragies de tous types sans majoration des thromboses
L’analyse approfondie des résultats secondaires confirme l'intérêt de la dose réduite, avec une réduction significative des complications hémorragiques cliniquement pertinentes par rapport à la dose complète (12,1 % vs 15,6 %, HR ajusté 0,75 ; IC à 95 % : 0,58-0,97 ; p=0,03). La fréquence des saignements majeurs est également plus faible avec la dose réduite (2,9 % contre 4,3 % en dose pleine). Concernant la mortalité globale, aucune différence significative n'est observée entre les deux groupes (17,7 % en dose réduite contre 19,6 % en dose pleine), la plupart des décès étant liés au cancer (84,5 % et 82,4 % des décès, respectivement).
Bien que la majorité des études cliniques portant sur l'anticoagulation chez les patients souffrant d'un cancer utilisent les saignements majeurs comme critère principal de tolérance, l'essai API-CAT a utilisé les saignements cliniquement pertinents, un composite de saignements majeurs ou de saignements non majeurs cliniquement pertinents. En outre, les chercheurs ont placé la barre très bas pour la notification des saignements non majeurs cliniquement pertinents en utilisant une liste de critères plus étendue que celle recommandée précédemment pour les études cliniques. Ce facteur doit être considéré comme une force car il reconnaît que dans cette population d'essai, dans laquelle plus de 80 % des patients avaient une maladie incurable, l'effet des saignements sur la qualité de vie globale primera souvent sur le fait que le saignement soit classé comme majeur ou non majeur.
Un nouveau standard de traitement
L’essai API-CAT, multicentrique, randomisé, en double aveugle, s’est déroulé sur une population représentative de patients cancéreux suivis pendant 12 mois après randomisation. La méthodologie robuste, incluant une adjudication centrale en aveugle des événements thromboemboliques et hémorragiques, renforce la validité des résultats. Toutefois, le critère élargi utilisé pour définir les saignements pertinents, intégrant des événements hémorragiques mineurs mais cliniquement significatifs pour les patients, constitue une originalité méthodologique et un atout pour la pratique clinique, même s'il diffère des standards habituels des grands essais antérieurs.
Selon un éditorial associé, ces résultats soutiennent un changement de paradigme dans la gestion à long terme de la MTEV associée au cancer. La réduction de l'incidence des saignements observée dans le groupe à dose réduite, sans faire progresser l'incidence des thromboembolies veineuses récurrentes, établit qu'apixaban, administré à une dose de 2,5 mg deux fois par jour, est un schéma approprié pour l'anticoagulation au-delà des 6 premiers mois chez les patients souffrant d'un cancer. Ce schéma posologique devrait être privilégié chez les patients traités pour cancer où le risque hémorragique est jugé important, ou lorsque l'impact du saignement sur la qualité de vie du patient constitue une préoccupation centrale. De futures études pourraient explorer davantage les profils spécifiques de patients (type et stade du cancer, traitements anticancéreux ou corticoïdes associés) qui bénéficieraient particulièrement de cette stratégie individualisée, pour affiner encore davantage l’équilibre bénéfice-risque.