Rhumatologie
Cancer, immunothérapie et arthrites : l’IRM objective trois phénotypes clés
En cas de cancer traité par immunothérapie, les arthralgies simples auraient le même risque articulaire que les arthrites inflammatoires cliniques, et l’IRM suggère une sous-évaluation pronostique par l’examen clinique seul. Trois tableaux émergent en imagerie : arthrite périphérique, syndrome pseudo-polyarthrite rhizomélique-like, et phénotype chevauchant avec un recours accru à l’immunomodulation dans le sous-groupe « arthrite périphérique ».
- semnic/istock
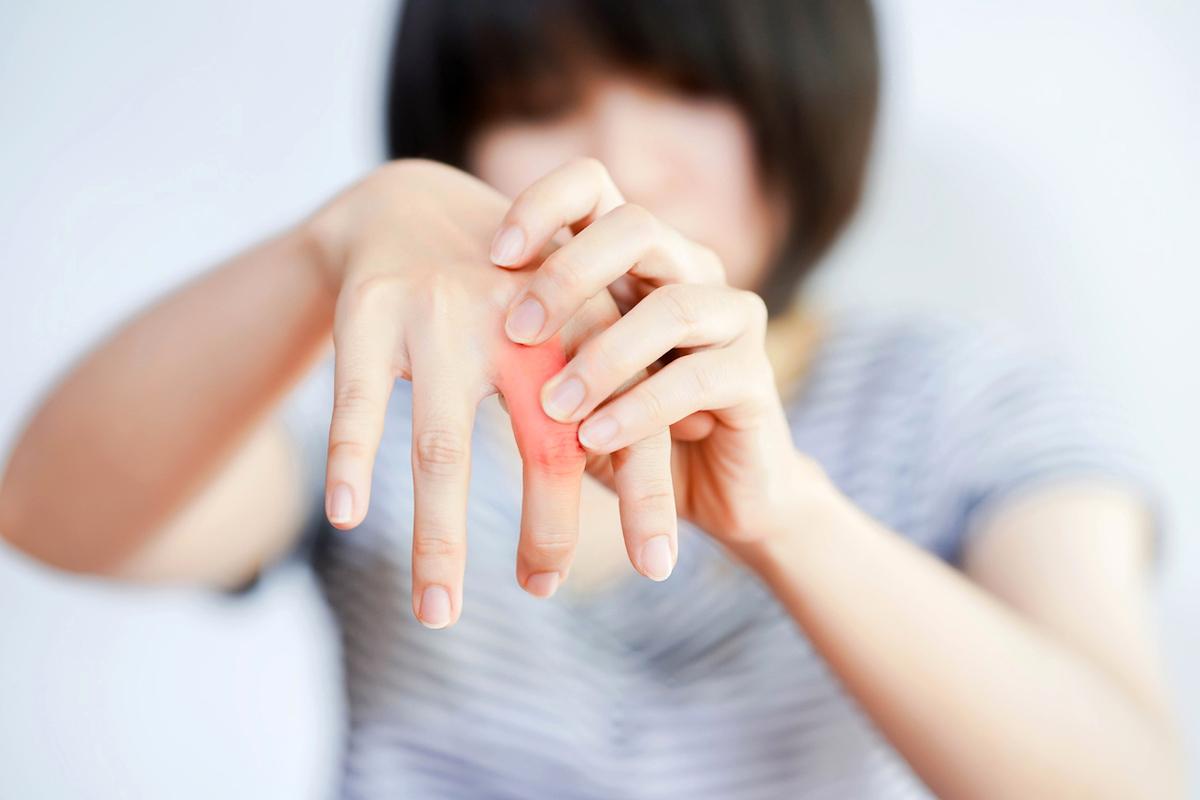
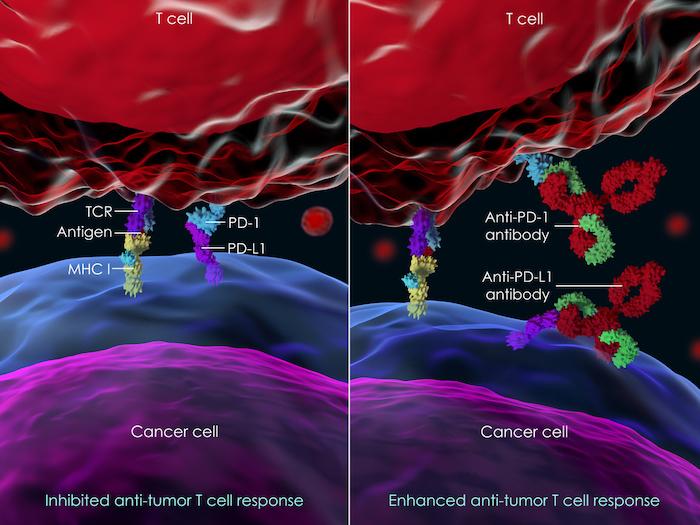
Les immunothérapies (inhibiteurs de checkpoints) ont transformé le pronostic de nombreux cancers mais exposent à des toxicités auto-immunes, dont les atteintes musculosquelettiques sont parmi les plus fréquentes (7% d’arthrite et arthralgies jusqu’à 43%). Les données cliniques publiées décrivent tantôt des polyarthrites distales « rhumatoïdes-like », tantôt des tableaux proximaux de type pseudopolyarthrite rhizomélique (PPR), voire des enthésites. L’hétérogénéité des phénotypes et la faible sensibilité de l’examen clinique nourrissaient l’hypothèse d’un fardeau inflammatoire sous-estimé.
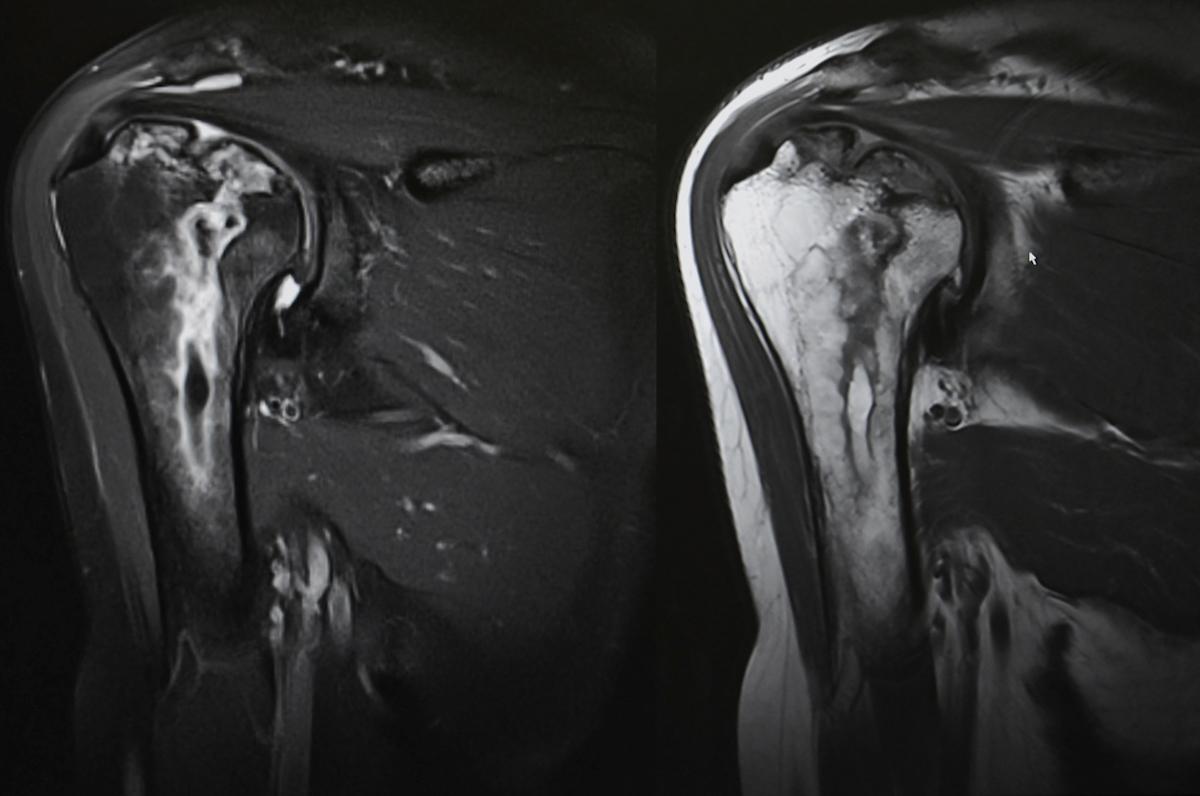
Une étude prospective conduite à Leeds a utilisé l’IRM corps entier avec gadolinium pour comparer l’imagerie de 60 patients adressés pour arthralgies (n=35) ou arthrite inflammatoire (n=25) débutant une immunothérapie ou dans les 6 mois, à 20 témoins sains. Deux lecteurs indépendants, en aveugle, ont scoré synovites, ténosynovites, bursites, enthésites, érosions et atteintes rachidiennes.
Selon les résultats publiés dans The Lancet Rheumatology, les scores médians de synovite, ténosynovite, enthésite et d’érosions sont significativement plus élevés chez les patients exposés aux immunothérapies que chez les témoins, sans différence entre les sous-groupes « arthralgie » et « arthrite ». Les articulations acromio-claviculaires (77 %), gléno-humérales (75 %), poignets (73 %) et métacarpo-phalangiennes (59 %) sont les sites les plus souvent inflammatoires. Trois patterns d’atteinte musculosquelettique sous immunothérapie se dégagent : arthrite périphérique (37 %), pseudo-polyarthrite rhizomélique-like (12 %), et chevauchement PPR-like/arthrite périphérique (20 %). L’atteinte axiale est rare (un seul cas), soulignant la primauté d’un processus périphérique.
Au-delà du signal : implications cliniques et tolérance
L’observation d’érosions dès la première évaluation IRM dans les deux phénotypes cliniques interpelle sur le potentiel destructeur de ces toxicités, même en l’absence d’articulation cliniquement gonflée. Les patients classés « arthrite périphérique » ont le plus souvent recours aux corticoïdes (initial et prolongé), et 4 sur 5 des prescriptions de DMARD (classiques ou ciblés) surviennent dans ce groupe, suggérant un profil plus sévère et plus exigeant en immunomodulation. À l’inverse, les tableaux pseudo-polyarthrite rhizomélique-like isolés sont moins consommateurs de DMARD, bien que les chevauchements soient fréquents et susceptibles d’évoluer vers des formes périphériques.
L’absence de différence de charge inflammatoire IRM entre « arthralgie » et « arthrite » remet en question une stratégie qui réserverait l’immunosuppression aux seuls patients avec synovite objectivée à l’examen, et plaide pour intégrer l’imagerie lorsque la symptomatologie est sévère ou invalidante. Toutefois, toute décision d’escalade thérapeutique doit équilibrer contrôle de la toxicité et préservation de l’efficacité antitumorale.
Cartographier l’inflammation pour mieux décider
Il s’agit d’une étude prospective monocentrique, avec lectures en aveugle et un protocole d’IRM corps entier couvrant membres, ceintures, rachis et structures péri-articulaires, comparée à des témoins sains appariés d’âge. La méthodologie renforce la validité interne pour caractériser le potentiel lésionnel sous immunothérapie ; la diversité tumorale et thérapeutique reflète la vraie vie, mais la recrutement spécialisé (rhumatologie de recours) peut sur-représenter des formes inflammatoires franches. Le nombre de malades et la durée de suivi limitent l’estimation des trajectoires à long terme et des corrélats pronostiques (destruction, chronicité), et invitent à des validations externes multicentriques.
Selon un commentaire d’expert associé, ces résultats soutiennent trois inflexions stratégiques. Il est tout d’abord nécessaire d’abaisser le seuil d’imagerie (idéalement IRM corps entier ou, à défaut, protocoles régionaux ciblant épaules, poignets et mains) chez les patients avec arthralgies sévères post-immunothérapie. Il faut ensuite stratifier la prise en charge selon le pattern IRM en anticipant les besoins supplémentaires en DMARD dans les formes périphériques étendues. Enfin, il est nécessaire de co-décider avec l’oncologue en documentant objectivement l’inflammation (IRM ou échographie) pour ajuster au plus juste corticoïdes et DMARD sans compromettre la réponse tumorale.
Les priorités de recherche incluent une classification fondée sur l’imagerie et la biologie, l’évaluation de seuils IRM prédictifs de réponse/chronification, et des essais contrôlés testant parcours thérapeutiques gradués intégrant l’IRM précoce.