Hématologie
Lymphome B diffus à grandes cellules en rechute : résultats prometteurs pour le glofitamab
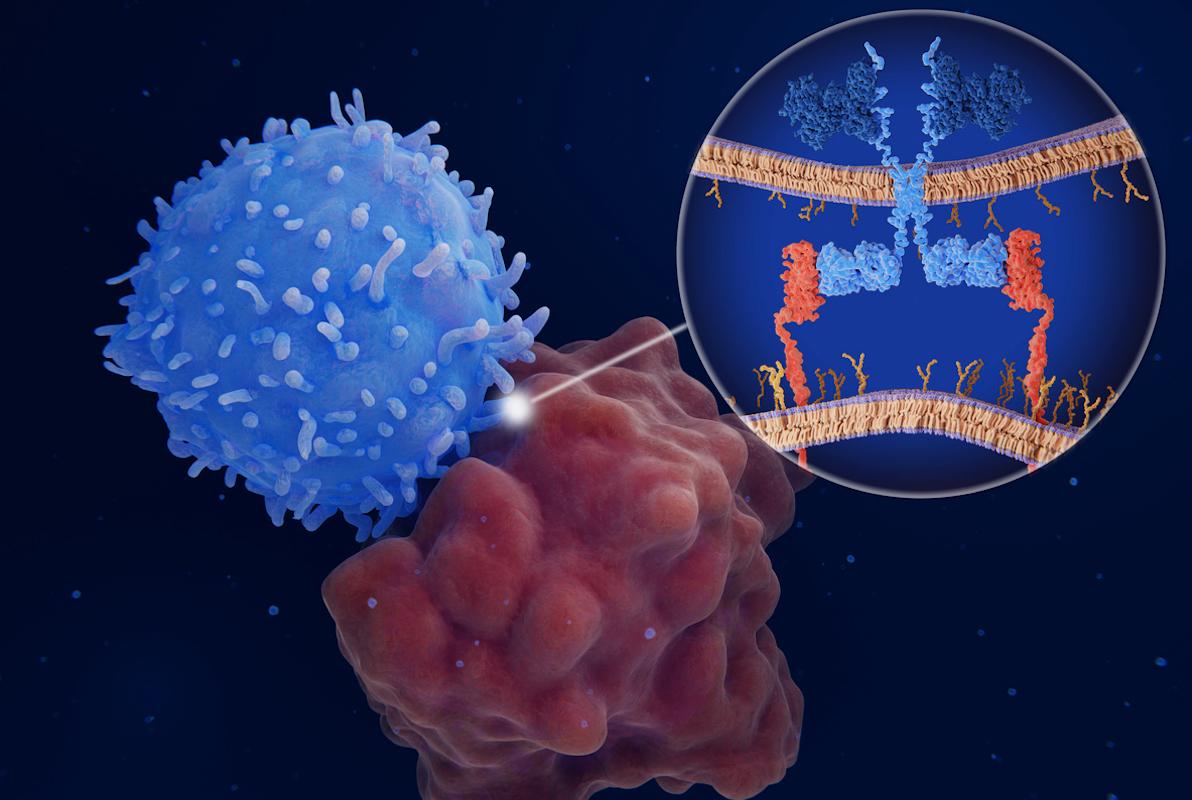
Si les CAR T-cells ont révolutionné le devenir des patients atteints de lymphome B diffus à grandes cellules (LBDGC), leur délai de fabrication les rendent inaccessibles pour certains patients. En conséquence, des traitements « on the shelf » tels que les anticorps bispécifiques représentent des perspectives prometteuses dans ce contexte clinique. Cet article décrit les données cliniques d’une phase 2 évaluant le glofitamab (anticorps anti-CD20 x CD3) chez des patients atteints de LBDGC en rechute.
- Gilnature/istock
Au décours d’une première ligne de traitement par immunochimiothérapie R-CHOP, 35 à 40% des patients présenteront une rechute ou un état réfractaire1. Le devenir de ces patients dépend alors de la faisabilité d’une autogreffe de cellules souches avec de mauvais résultats en cas d’inéligibilité et de rechutes répétées2.
Bien que les thérapies par CAR T-cells semblent être les plus efficaces pour les patients atteints de LBDGC en situation de rechute et/ou réfractaire après ≥2 lignes de traitement, elles ne sont pas toujours accessibles (contraintes logistiques, géographiques ou d'approvisionnement) et seulement 40% des patients obtiennent une réponse durable au décours3.
Dans ce contexte, les auteurs ont évalué le glofitamab, un anticorps bispécifique antiCD20 x CD3, chez des patients atteints de LBDGC en rechute et/ou réfractaire4.
Une population de LBDGC de stade avancé et réfractaires
Entre janvier 2020 et septembre 2021, 155 patients ayant reçu ≥2 lignes de traitement ont été inclus pour recevoir le glofitamab en monothérapie (doses progressives de 2,5 mg et 10 mg, puis 30 mg au J1 de C2 à C12), au décours d’un prétraitement par obinutuzumab (réduction du risque de syndrome de relargage de cytokines (SRC)). L'âge médian était de 66 ans (21-90).
Cent dix patients (71%) avaient un LBDGC (non-spécifié), 27 (18%) un lymphome folliculaire transformé, 11 (7%) un lymphome à cellules B de haut grade et 6 (4%) un lymphome primitif du médiastin. Les patients avaient reçu une médiane de trois lignes de traitements antérieurs et 33% avaient déjà reçu une thérapie par CAR T-cells (dont 89% étaient réfractaires). La majorité des patients étaient de stade avancé (stade III/IV pour 75%) et présentaient une maladie réfractaire : réfractaire primaire pour 58% et réfractaire au dernier traitement pour 86%.
Une efficacité prometteuse en monothérapie
Avec 12,6 mois de suivi médian, et une médiane de 5 cycles de glofitamab reçus (médiane de 79 jours), 39% des patients (95%CI, 32 – 48) ont eu une réponse complète. Le délai médian d’obtention d’une réponse complète est de 42 jours (95%CI, 42 - 44) avec des résultats comparables chez les patients ayant préalablement reçu des CAR T-cells (35% de réponse complète contre 42% pour les autres patients).
Les réponses complètes persistent à 12 mois pour 78% des patients (95%CI, 64 - 91), tandis que les survies sans progression et globale à 12 mois était respectivement de 37% (95%CI, 28 - 46) et 50% (95%CI, 41 – 58).
Un syndrome de relargage cytokinique inaugural
Le SRC, événement indésirable le plus fréquent (63%), survient principalement lors des premières doses de glofitamab (délai médian de 13,5 heures après C1J8, pour une durée médiane de 30,5 heures). Les SRC étaient principalement de faible grade (47% de grade 1, 12% de grade 2, 3% de grade 3 et 1% de grade 4).
Des événements indésirables neurologiques (dysphonie, état confusionnel, désorientation), compatibles avec un ICANS, survenaient chez 8% des patients (3% de grade ≥3) et étaient résolutifs. Finalement, les infections survenaient chez 38% des patients (dont 15% de grade ≥3), majoritairement liées à la pandémie Covid-19. Au total, 9% des patients interrompaient le traitement en raison des effets indésirables.
Conclusion
Du fait de son efficacité, de son accessibilité immédiate et d’un schéma à durée fixe, le glofitamab représente une alternative thérapeutique prometteuse pour les patients atteints de LBDGC de mauvais pronostic et ayant reçu ≥ 2 lignes de traitement antérieures. Cet anticorps bispécifique ouvre également la voie à des séquences thérapeutiques de bridging vers une allogreffe ou des CAR T-cells (9 patients de l’étude traités avec succès).
Références
- Sehn LH, Gascoyne RD. Diffuse large B-cell lymphoma: optimizing outcome in the context of clinical and biologic heterogeneity. Blood 2015;125:22-32.
- Crump M, Neelapu SS, Farooq U, et al. Outcomes in refractory diffuse large B-cell lymphoma: results from the international SCHOLAR-1 study. Blood 2017;130:1800-8.
- Roschewski M, Longo DL, Wilson WH. CAR T-Cell Therapy for Large B-Cell Lymphoma - Who, When, and How? N Engl J Med 2022;386:692-6.
- Dickinson MJ, Carlo-Stella C, Morschhauser F, et al. Glofitamab for Relapsed or Refractory Diffuse Large B-Cell Lymphoma. N Engl J Med 2022;387:2220-31.