Onco-Thoracique
Cancer Bronchique à Petites Cellules (CBPC) : un bisphecific T cell Engager en phase II
Dans le Cancer Bronchique à Petites Cellules, une nouvelle immunothérapie à base d'anticorps bispécifique "T Cell Engager" est testée en phase II.
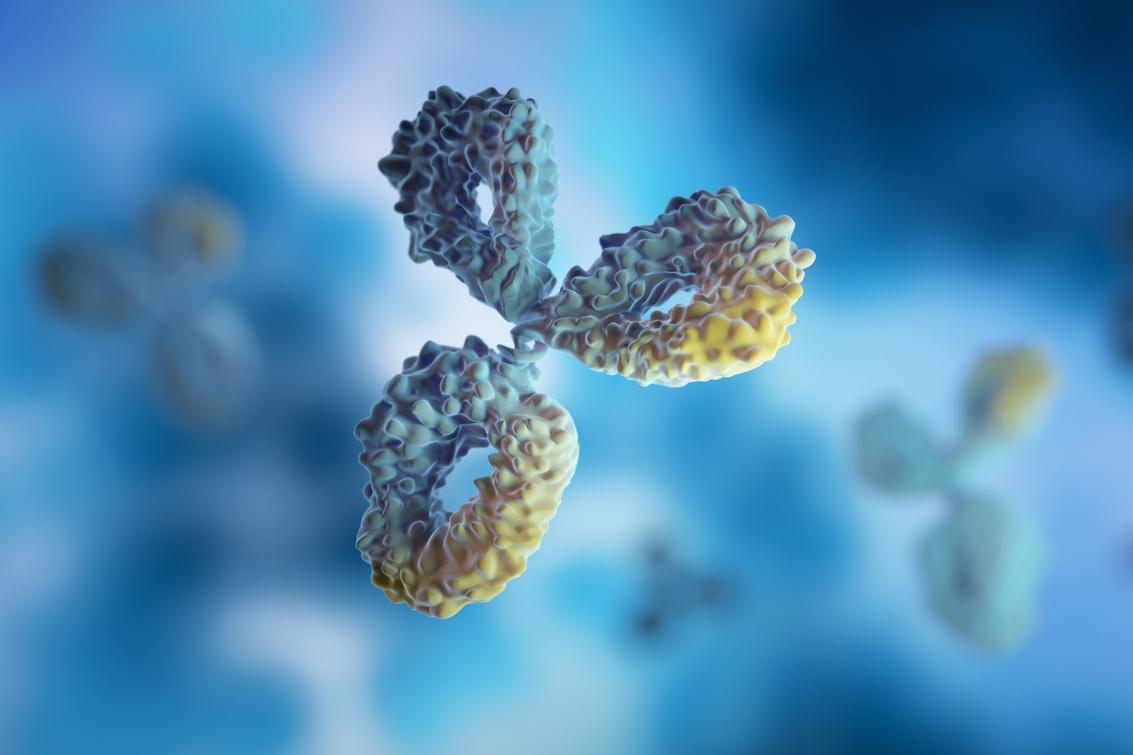
- peterschreiber.media/iStock
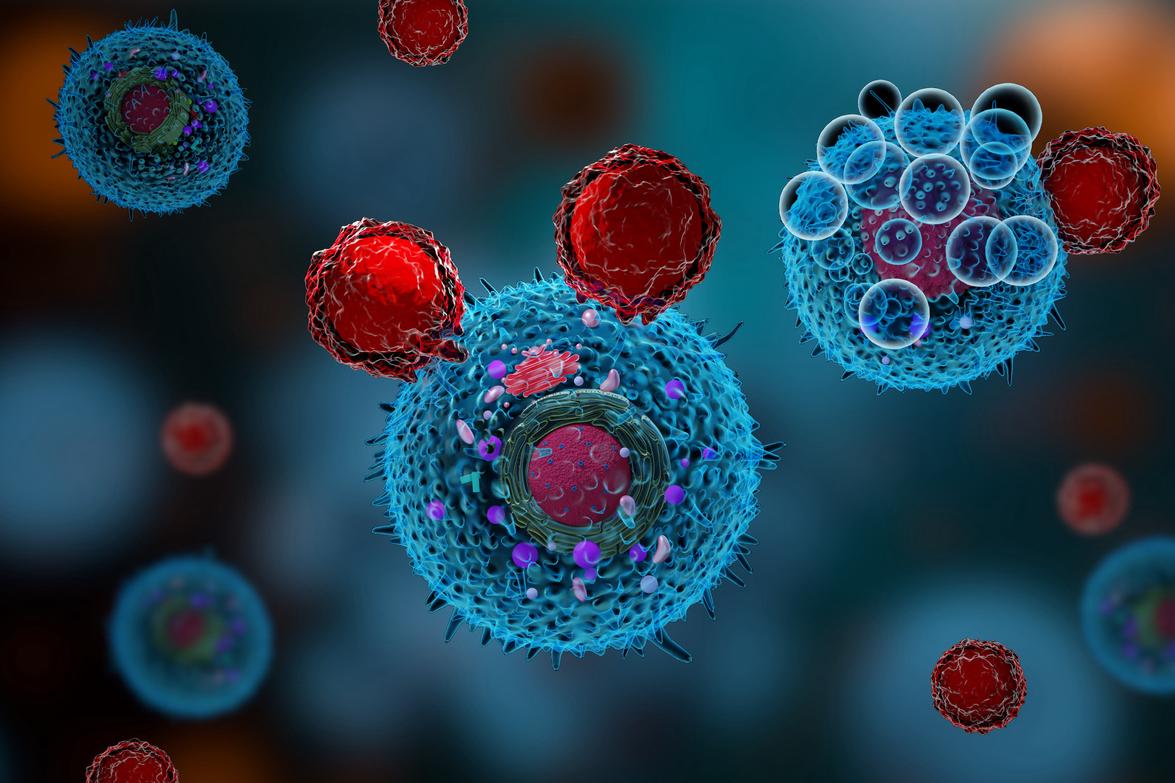
Le Tarlatamab, immunothérapie innovante appartenant au « T cell engager », est un anticorps bispécifique qui a pour objectif de rapprocher de par sa bispécificité : d’une part les cellules exprimant le DLL3 (antigène exprimé par les cellules tumorales du Cancer Bronchique à Petites Cellules ou CBPC), et d’autre part le CD3 exprimé par les lymphocytes T dont les lymphocytes T CD8 cytotoxiques.
Il a été montré que le gène de l’antigène DLL3 est exprimé par 85 à 94 % des patients avec un CBPC. Le fait de rapprocher les lymphocytes T des cellules tumorales a pour objectif de favoriser l’action des lymphocytes T CD8 cytotoxiques envers les cellules tumorales.
DELLphi-301 teste le Tarlatamab en phase II dans le CBPC
L’essai DELLphi-301 est un essai de phase II évaluant l’efficacité antitumorale ainsi que la tolérance du tarlatamab, administré tous les 15 jours. Deux schémas de dose étaient évalués : 10 mg ou 100 mg en injection intraveineuse, chez des patients précédemment traités pour un CBPC métastatique.
Au total 220 patients ont reçu du Tarlatamab, après une médiane de 2 lignes de traitement. La médiane de suivi était de 10 mois dans les 2 bras de dose. Une réponse objective a été observée chez 40 % des patients dans le bras 10 mg et chez 32 % des patients dans le bras 100 mg. Parmi les patients qui ont présenté une réponse objective, la durée de la réponse était d’au moins 6 mois chez 59 % des patients.
Au moment de l’analyse, 55 % des patients appartenant au groupe 10 mg était en réponse objective versus 57 % dans le bras 100 mg. La médiane de survie sans progression était de 4,9 mois [IC95 % : 2,9-6,7] dans le groupe 10 mg versus 3,9 mois [IC 95 % : 2,6-4,4] dans le groupe 100 mg. Le taux de survie à 9 mois était de 68 % et 66 % respectivement dans les bras 10 mg et 100 mg.
Un syndrome de relargage cytokinique non négligeable
Les évènements indésirables rencontrés ont été : la survenue d’syndrome de relargage cytokinique (51 % des patients dans le groupe 10 mg versus 61 % dans le groupe 100 mg), l’anorexie (29 % versus 44 % respectivement), et un syndrome fébrile (35 % versus 33 %). Le syndrome de relargage cytokinique a été observé principalement lors du premier cycle de traitement.
En conclusion, le Tarlatamab administré à la dose de 10 mg tous les 15 jours a montré un bénéfice en terme de réponse tumorale. Le syndrome de relargage cytokinique à l’introduction du traitement doit être anticipé principalement à la première injection. Ce traitement est encourageant et, promet l’arrivée de nouvelles immunothérapies sur le marché dans la prise en charge du Cancer Bronchique à Petites Cellules.


-1692873376.jpg)