Hémochromatose : l'excès de fer peut nuire à la santé

L’hémochromatose est une maladie d’origine génétique qui entraîne une absorption excessive du fer alimentaire et un dépôt dans de nombreux organes. La maladie évolue insidieusement et, si elle n’est pas traitée, peut conduire à des atteintes de divers organes (cirrhose, cancer du foie, insuffisance cardiaque...).
Des mots pour les maux
L’hémochromatose est une maladie génétique liée à l’altération (mutation) d’un ou de plusieurs gènes impliqués dans l’absorption du fer : il s’agit donc d’une maladie transmissible.
Les gènes sont des petites parties (séquences) des chromosomes (contenus dans le noyau des cellules) qui portent l’information nécessaire à la synthèse de différentes protéines et enzymes.
Du fait de l’anomalie génétique, l’absorption du fer est augmentée et l’accumulation de ce métal dans différents organes conduit insidieusement à leur altération.
La maladie peut se révéler par une fatigue, une coloration anormale de la peau, un diabète, une cirrhose hépatique et une insuffisance cardiaque.
Qu'est-ce que l’hémochromatose ?
L’hémochromatose est une maladie de surcharge en fer de l’organisme qui est due à une absorption excessive du fer alimentaire dans l’intestin. Il s’agit d’une maladie chronique qui évolue insidieusement et qui peut conduire à des altérations de divers organes si elle n’est pas traitée.
L’absorption du fer, qui est normalement régulée, ne l’est plus dans l’hémochromatose où il existe une anomalie génétique, c’est-à-dire une altération (mutation), d’un ou de plusieurs gènes qui commandent cette régulation.
Il existe plusieurs types d’hémochromatose selon la mutation en cause. Les différentes mutations semblent correspondre à des profils cliniques particuliers (signes cliniques et gravité) de la maladie.
L’hyper-absorption intestinale du fer entraîne l’accumulation en trop grandes quantités de ce métal essentiel pour l'organisme et en particulier dans le foie, les glandes hormonales, le cœur, les articulations…). Cette surcharge en fer peut conduire à des altérations graves de ces organes (cirrhose, cancer du foie, insuffisance cardiaque...) et, à l’extrême, conduire à une mort prématurée.
Quels sont les signes de l’hémochromatose ?
Les hommes sont plus souvent atteints par cette maladie que les femmes (3 hommes atteints pour 1 femme). Les premiers signes de la maladie apparaissent le plus souvent après 40 ans, mais certaines formes d’hémochromatose juvénile peuvent débuter entre 5 et 30 ans.
L'hémochromatose entraîne souvent une fatigue chronique, une coloration foncée de la peau (aussi appelée « mélanodermie » par les médecins), ainsi qu’une atteinte du foie, du pancréas, des articulations, des os, des glandes endocrines ou du cœur.
Ce sont ces atteintes d’organes qui sont à l’origine des différentes complications observées à l'âge adulte telles qu'une cirrhose (fibrose hépatique) avec le risque de cancer du foie (carcinome hépatocellulaire), un diabète insulino-dépendant (c’est-à-dire par insuffisance de sécrétion en insuline par le pancréas), une arthrose touchant plusieurs articulations (polyarthrose liée à des dépôts de fer dans le cartilage), une ostéoporose en rapport avec un hypogonadisme hypogonadotrophique (insuffisance en hormones sexuelles comme les estrogènes et la testostérone) ou une insuffisance cardiaque.
Les anomalies caractéristiques de la maladie qui sont observées dans le sang comprennent une élévation du coefficient de saturation de la transferrine et du taux de ferritine sérique. Certaines formes d’hémochromatose évoluent à très bas bruit, sans signe clinique apparent (asymptomatiques) avec des caractéristiques biologiques particulières marquées par l'association d'un taux élevé de ferritine sérique et d'un coefficient de saturation de la transferrine normal ou bas.
L’hémochromatose est-elle héréditaire ?
L’hémochromatose familiale se transmet sur le mode autosomique récessif : cela veut dire que seuls sont atteints les enfants qui ont reçu le gène altéré (muté), à la fois de leur père et de leur mère. Ainsi, les personnes atteintes sont porteuses du gène muté en deux exemplaires (elles sont dites homozygotes) alors que chacun des parents n’en est porteur qu’à un seul exemplaire (ils sont dits hétérozygotes).
Cette maladie ne touche donc habituellement que des frères et sœurs dans une même famille. La probabilité d’avoir un autre enfant atteint d’hémochromatose familiale est de 1 sur 4 pour un couple ayant déjà donné naissance à un enfant malade.
Une forme particulière d’hémochromatose, celle de type 4, se transmet sur le mode autosomique dominant, c’est-à-dire systématiquement de génération en génération, avec, à chaque grossesse, un risque sur deux de transmettre la maladie.
Le conseil génétique peut être proposé aux familles atteintes par cette maladie afin de les informer sur le risque de transmettre la mutation responsable de la maladie.
Quels sont les différents types d’hémochromatose ?
La forme la plus fréquente de la maladie est l’hémochromatose héréditaire de type 1 (ou HFE). Elle est due à une mutation du gène HFE qui est situé sur le chromosome 6. Deux types d’altérations existent : la mutation C282Y et la mutation H63D.
D’autres formes d’hémochromatose moins fréquentes existent.
• L’hémochromatose juvénile, ou hémochromatose de type 2, plus rare, est due soit à une mutation sur le chromosome 1 (hémochromatose juvénile type 2A) soit à celle du gène de l’hepcidine (protéine active sur le métabolisme du fer récemment découverte) sur le chromosome 19 (hémochromatose juvénile type 2B).
• L’hémochromatose de type 3 résulte d’une mutation du gène du récepteur 2 de la transferrine (TFR2) au niveau du chromosome 7. L’hémochromatose de type 4 est due à une mutation du gène codant pour la ferroportine sur le chromosome 2.
Qui peut être atteint par la maladie ?
L’hémochromatose est surtout observée dans les populations d’Europe du Nord ou d’Amérique du Nord. En France, la maladie est observée dans un cas pour deux à trois cents personnes. Elle est surtout présente en Bretagne et dans le département du Gard.
Toutes les personnes qui sont porteuses de la mutation ne développent pas une hémochromatose clinique. En effet, pour que la maladie apparaisse, il est nécessaire que la mutation responsable se trouve sur les deux chromosomes de la paire de chromosome concernée (homozygote), ce qui est relativement rare. Si la personne ne porte la mutation que sur un seul de ses 2 chromosomes appariés (hétérozygote), la maladie ne se développera que si d’autres facteurs favorisant l’accumulation du fer dans l’organisme sont aussi présents : par exemple, en cas d’alcoolisme associé.
Les hommes sont plus fréquemment atteints d’hémochromatose symptomatique que les femmes. Une des explications tient au fait que les règles et la grossesse représentent une cause de perte régulière de fer qui tend à retarder l’apparition des symptômes d’hémochromatose.
Quand doit-on évoquer une hémochromatose ?
L’hémochromatose familiale est une maladie chronique qui évolue très progressivement et très lentement, ce qui est responsable d’un retard diagnostic fréquent. Ce retard est largement préjudiciable pour les personnes atteintes, car le traitement est surtout efficace en cas de surcharge simple, avant l’installation d’une souffrance des différents organes où se font les dépôts.
Le diagnostic peut donc être évoqué selon différents tableaux qui sont présents en fonction de l’âge :
• Entre 0 et 20 ans, l’accumulation de fer dans l’organisme n’est pas très importante et ne donne pas de symptômes (sauf dans les formes juvéniles exceptionnelles).
La seule façon d’évoquer le diagnostic est de faire un dépistage génétique dans les familles atteintes.
• Entre 20 et 40 ans, il existe une surcharge de fer avérée, y compris dans les organes habituellement touchés, mais comme le dépôt en fer est très progressif, il n’y a pas toujours de manifestations cliniques.
Si la maladie n’est pas décelée et si elle n’est pas traitée, elle va progresser vers le stade des altérations débutantes des organes avec l’apparition de signes ou symptômes.
• Les manifestations cliniques apparaissent vers l’âge de 35 ans chez l’homme et plus tardivement chez la femme, vers l’âge de 45 à 50 ans.
A la phase d’état, la maladie se traduit souvent par une fatigue chronique marquée.
Des douleurs articulaires peuvent survenir, touchant volontiers les petites articulations des doigts, avec des douleurs lors de la poignée de main, ou d’autres articulations plus importantes, telles que les poignets ou les hanches.
Plus tardivement, un brunissement de la peau (mélanodermie) apparaît très souvent : il s’agit d’un aspect «grisâtre, métallique» de la peau qui intéresse le visage, les grosses articulations, et les organes génitaux. La peau s’affine (atrophie) avec l’apparition d’un aspect squameux ou en écailles de poisson (ichtyose) et une raréfaction des cheveux et des poils pubiens.
© Inserm/Belin, Marie-Françoise
http://www.serimedis.inserm.fr
• Lorsque le diagnostic est retardé, les complications apparaissent qui se traduisent par des manifestations cliniques qualifiées de tardives qui concernent le foie, les glandes endocrines ou le cœur.
Le volume du foie est augmenté, ce qui peut provoquer des douleurs abdominales. Les fonctions assurées normalement par le foie se détériorent au fur et à mesure que la cirrhose s’installe. La cirrhose elle-même expose au risque de développer un cancer du foie (carcinome hépatocellulaire).
Sur le plan hormonal, un diabète peut survenir. On parle de « diabète bronzé » car il s’associe au brunissement de la peau. Parfois, il y a d’autres glandes endocrines atteintes avec diminution de la production des hormones correspondantes. Ainsi, une impuissance secondaire à une atteinte des testicules peut apparaître. Plus rarement, l’atteinte de l’hypophyse, petite glande sous le cerveau qui commande la sécrétion de nombreuses hormones, entraîne un défaut de sécrétion de toutes les glandes.
Le cœur peut également être touché avec une augmentation de son volume, un trouble de la contraction du muscle cardiaque et des signes d’insuffisance cardiaque : essoufflement, palpitations, froideur des extrémités. A l’effort, ces signes s’accompagnent d’une coloration bleuâtre de la peau (cyanose) témoignant de l’insuffisance en oxygénation des tissus. Cette insuffisance cardiaque peut toucher le cœur droit, ce qui gêne le retour du sang vers le cœur et provoque un engorgement du foie avec des douleurs sous les côtes droites. Parfois l’atteinte du cœur se traduit par un rythme cardiaque irrégulier (trouble du rythme).
Au stade tardif de la maladie, qui est devenu exceptionnel, on constate l’association d’un diabète, d’une insuffisance cardiaque (parfois avec arythmie), d’une polyarthrose, d’une ostéoporose et d’une cirrhose hépatique chez un malade dont la coloration de la peau est sombre alors qu’elle était normale auparavant.
Comment faire le diagnostic ?
Chez une personne qui se plaint de signes évocateurs de la maladie, le diagnostic est posé grâce à quelques examens sanguins.
Le taux de fer dans le sang (fer sérique) est très élevé (supérieur à 30 μmol/l).
Cette augmentation à elle seule ne permet pas le diagnostic qui ne peut être affirmé que s’il s’y associe une élévation du coefficient de saturation de la transferrine (protéine de transport du fer dans le sang) : taux supérieur à 50 %. La détermination du coefficient de saturation de la transferrine est donc l’examen déterminant.
Le dosage de la ferritine (reflet des réserves de fer dans l’organisme) montre également des valeurs très élevées.
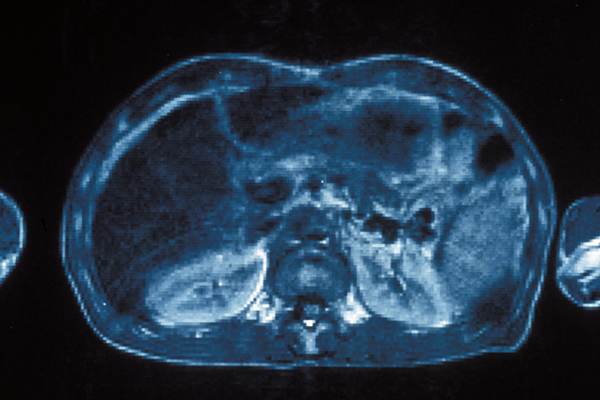
La preuve de la surcharge du foie en fer (hépatosidérose), qui nécessitait autrefois une biopsie du foie pour être mise en évidence, est actuellement faite grâce l’imagerie par résonance magnétique (IRM).
Un test génétique, le test HFE (mise en évidence de la mutation du gène HFE) a aujourd’hui une place privilégiée dans le diagnostic de l’hémochromatose. Sa positivité est en effet un très fort argument pour confirmer le diagnostic.
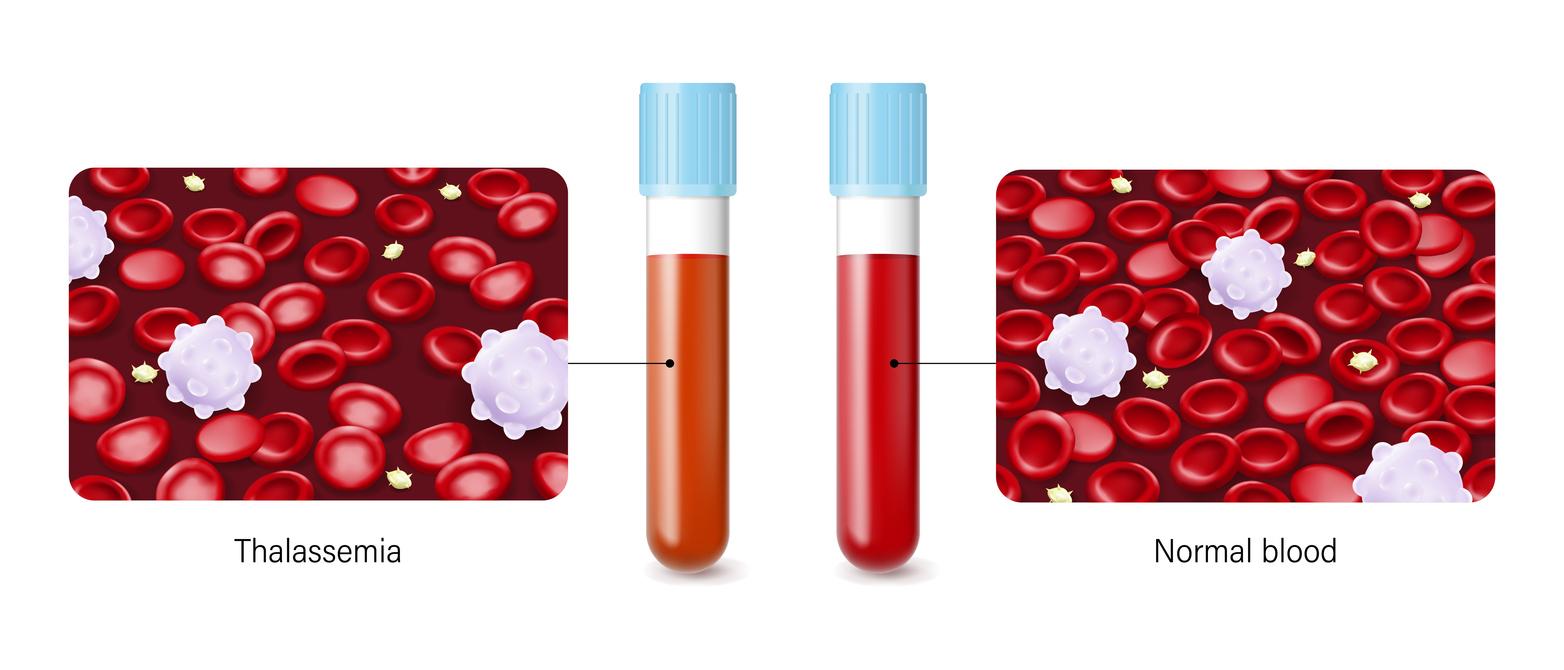
Le diagnostic d’hémochromatose n’est cependant sûr qu’après avoir éliminé les autres causes de surcharge en fer comme certaines maladies du sang (thalassémies), une cirrhose alcoolique et certaines maladies métaboliques qui nécessiteront d’autres examens de sang.
Faut-il faire une biopsie hépatique ?
La biopsie du foie consiste en un prélèvement sous anesthésie locale d’un petit morceau de foie. Elle est obtenue par ponction sous les côtes droites avec une aiguille.
Elle a été longtemps indispensable pour montrer la surcharge en fer du foie. Elle n’est actuellement plus nécessaire pour poser le diagnostic.
La biopsie hépatique n’a actuellement d’intérêt que pour rechercher une complication de la surcharge en fer comme la cirrhose du foie : elle est réservée aux cas où la progression vers le cancer du foie est suspectée.
D’autres examens sont-ils nécessaires ?
Quand le diagnostic d’hémochromatose est posé, il est nécessaire de réaliser une évaluation de la fonction des différents organes susceptibles d’être atteints.
C’est ainsi que des dosages des transaminases, de la glycémie, de la testostéronémie (chez l’homme), une ostéodensitométrie (en raison du risque d’ostéoporose) et une échocardiographie pourront être demandés par le médecin.
Est-il possible de faire un dépistage familial ?
Dépistée tôt, l’hémochromatose peut bénéficier de traitements qui en ralentissent l’évolution et préviennent ses complications. Mais, comme l’hémochromatose est une maladie qui évolue très lentement et en silence et comme elle se manifeste par des signes très variables d’une personne à l’autre, le délai entre les premiers symptômes et le diagnostic est parfois de plusieurs années : ceci aboutit fréquemment à un diagnostic tardif, au stade des complications.
Les membres de la famille d’une personne atteinte d’hémochromatose doivent donc bénéficier d’une détermination du coefficient de saturation de la transferrine et d’un test génétique afin de rechercher l’anomalie génétique. Ces tests se font par simple prise de sang.
Dans le nord de l’Europe, la mutation C282Y est présente dans 93-95 % des hémochromatoses et permet ainsi le dépistage de cette maladie via la recherche de cette anomalie dans cette partie du monde.
Quel est le traitement de l’hémochromatose ?
Le traitement de l’hémochromatose vise à réduire la quantité de fer en surcharge dans le corps.
Pour cela, le médecin prescrit des saignées (« phlébotomies »), c’est-à-dire des prélèvements réguliers de sang. En effet, aucun régime alimentaire ne permet, à lui seul, d’éviter ou de limiter la surcharge en fer, ni d’ailleurs le nombre de saignées.
De la même manière que pour un don du sang, le malade est installé en position allongée avec un matériel de prélèvement stérile pour lui prélever du sang. Il est recommandé de boire abondamment pendant la saignée pour compenser la perte liquidienne occasionnée.
Les saignées ne guérissent pas définitivement l’hémochromatose : elles ne font que compenser l’absorption excessive de fer par l’intestin. Si elles sont réalisées régulièrement, elles permettent de stabiliser les taux de fer à des valeurs normales.
Au départ, une saignée par semaine est nécessaire. Elle permet de prélever environ 400 ml de sang chez la femme et 500 ml chez l’homme en une vingtaine de minutes (en règle générale, on prélève 7 ml par kg de poids).
Ces saignées hebdomadaires sont maintenues tant que persiste la surcharge en fer. Dès que le taux sanguin de ferritine devient inférieur à 50 μg/L, elles deviennent mensuelles ou trimestrielles selon les cas, de manière à maintenir la
férritinémie au-dessous de 50 μg/L. Les saignées seront maintenues à vie.
Chez la femme enceinte, les saignées sont arrêtées pendant toute la grossesse. La supplémentation en fer n’est pas nécessaire.
Lorsque le diagnostic de l’hémochromatose a été fait avant ou au début de l’apparition des symptômes, le traitement par saignée est efficace et procure une espérance et une qualité de vie normales.
Bien sûr, en cas de maladies associées, comme une arthrose, une insuffisance cardiaque, un diabète... il faudra les traiter également car elles évoluent pour leur propre compte.
Quelles sont les conséquences pour la vie du malade ?
L’hémochromatose, diagnostiquée et traitée précocement, ne présente aucun retentissement sur la qualité de vie des malades, en dehors de l’obligation d’effectuer les saignées, 4 à 6 fois par an en traitement d’entretien. Les saignées pouvant être effectuées à domicile, le malade peut donc mener une vie tout à fait normale.
Il est recommandé aux personnes souffrant d’hémochromatose de se faire vacciner contre l’hépatite B afin d’éviter les complications liées à une éventuelle hépatite chronique provoquée par le virus de l’hépatite B. De plus, la recherche systématique d’une éventuelle infection par le virus de l’hépatite C est effectuée (il n’existe pas de vaccin contre cette maladie).
Du fait de leur toxicité potentielle sur le foie, le paracétamol et les corticoïdes (dérivés de la cortisone) doivent dans la mesure du possible, être évités chez les personnes souffrant d’hémochromatose, par exemple en cas de douleurs ou de fièvre.
Il est aussi recommandé d’éviter les excès de boissons alcoolisées du fait de leur toxicité pour le foie.
Faut-il suivre un régime alimentaire ?
Aucun régime alimentaire particulier n’est nécessaire, en revanche, il est indispensable de limiter les apports en boissons alcoolisées car il existe un risque plus élevé de cirrhose ou de cancer du foie.
De la même façon, il ne jamais prendre de suppléments de fer (qui sont parfois présents dans les compléments multivitaminiques).
Comment se faire suivre ?
Le suivi et les saignées (4 à 6 fois par an) peuvent se faire au niveau de toutes les consultations d’hépatologie et de gastroentérologie, voire à domicile.
Le conseil génétique permet de dépister la maladie chez les personnes de la famille proche, et ce avant toute manifestation de la maladie.
Les coordonnées des consultations de génétique pour l’hémochromatose sont disponibles sur le site Orphanet (www.orpha.net).
Peut-on bénéficier d’aide en cas de maladie ?
En France, l’hémochromatose dans ses formes avancées, fait partie des 30 affections longue durée (ALD 30) qui donnent lieu à exonération du ticket modérateur c’est-à-dire au remboursement à 100 % par la caisse de sécurité sociale des frais médicaux imputables à la maladie.
Dans les formes graves, les malades ont la possibilité d’obtenir une allocation d’adulte handicapé en déposant un dossier auprès de la Maison Départementale du Handicap.
L’hémochromatose en France
L’hémochromatose touche un Français sur 300 mais la moitié des patients ignore qu’ils en souffrent.
Sans traitement, elle représente un danger réel : l’hémochromatose entraîne des complications dans un cas sur trois et cause chaque année 524 cancers du foie.
Les liens de l’hémochromatose
Le site de l’Association Hémochromatose France
http://www.hemochromatose.fr/
Les consultations de génétique pour l’hémochromatose sur le site Orphanet
http://www.orpha.net
Les liens internes à Pourquoi Docteur
Hémochromatose : un malade sur deux s'ignore
Hémochromatose : dépister une maladie silencieuse
Arthrose : des douleurs sans lien obligé avec le vieillissement
Diabète de type 2 : une véritable épidémie mondiale
Ostéoporose : une maladie des os où il faut prévenir les fractures
Insuffisance cardiaque : un essoufflement peut aussi être lié à une maladie du cœur




















Commentaires
Ajouter un commentaire
commentaires