Diabétologie
Diabète de type 1 : le teplizumab, un anti-CD3, annonce une révolution aux Etats-Unis
Les États-Unis ont approuvé le teplizumab, un anticorps monoclonal anti-CD3 humanisé, le premier médicament qui permettrait de retarder la dépendance à l'insuline chez les personnes avec des anticorps anti-ilots de Langerhans et un trouble glucidique annonçant un diabète de type 1. Ce traitement pose désormais la question du dépistage de ce diabète.

- AlexRaths/iStock
C’est une avancée qui serait majeure pour le traitement et la prévention du diabète de type 1 : les régulateurs de l'agence américaine des médicaments, la Food and Drug Administration (FDA), ont approuvé le teplizumab, un anticorps monoclonal anti-CD3 humanisé, le premier traitement qui pourrait retarder pendant des années (2 ans en moyenne et jusqu'à 11 ans), l'apparition du diabète de type 1 pour les patients âgés de huit ans et plus.
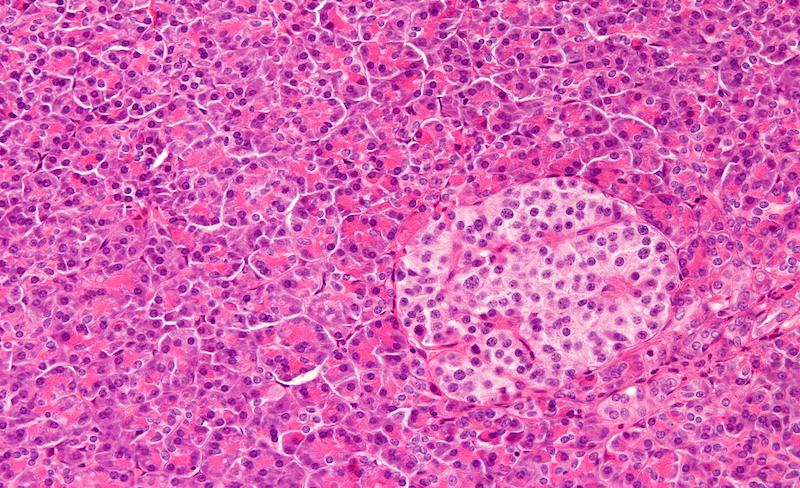
Le teplizumab sera utilisé pour traiter les enfants avec un risque élevé de diabète de type 1, c'est-à-dire ceux qui ont des anticorps indiquant une attaque immunitaire contre les ilots de cellules bêta dans leur pancréas et dont la tolérance au glucose n'est pas normale. Le traitement consiste en une perfusion de 14 jours du médicament, d'un anticorps monoclonal qui bloque les lymphocytes T, les empêchant d'attaquer les cellules productrices d'insuline du pancréas.
Un anti-CD3 pour prévenir le diabète de type 1
Ce médicament - vendu sous le nom de Tzield® - est un type d'immunothérapie, un anticorps monoclonal anti-CD3 humanisé, qui agit en s'attaquant à la cause immunologique du diabète de type 1. Le diabète de type 1 est une maladie auto-immune non évitable qui se développe généralement dans l'enfance mais il peut survenir à tout âge, indique l'Institut national de la santé et de la recherche médicale (Inserm).
Le teplizumab est fabriqué par Provention Bio, qui s'associera à Sanofi pour le commercialiser aux États-Unis sous le nom de marque Tzield. Lors d'une conférence téléphonique avec les investisseurs, Provention a déclaré que le médicament coûterait 13 850 dollars par flacon ou 193 900 dollars pour le traitement de 14 jours. La société a déclaré que le teplizumab devrait être disponible d'ici la fin de l'année.
Le diabète de type 1 bénéficierait d'une prévention
"Les complications concernent principalement le cœur et les vaisseaux, qui sont les premiers lésés par une concentration excessive et permanente de glucose dans le sang. Le diabète entraine ainsi des lésions vasculaires augmentant le risque d’athérosclérose, d’infarctus du myocarde, d’AVC ou encore d’artérite des membres inférieurs. Le diabète affecte également les petites artères qui nourrissent les reins, les nerfs des membres inférieurs et la rétine – on parle alors de complications micro-vasculaires”, indique l’Inserm.
Habituellement, les personnes atteintes de diabète de type 1 sont obligées de s'injecter régulièrement de l'insuline, une hormone essentielle à la régulation de la glycémie notamment dans les cellules musculaires, les adipocytes (cellules graisseuses) et les hépatocytes (cellules du foie). L’absence de cette hormone empêche l’organisme de stocker du sucre. Elle entraîne donc un risque majeur d’hyperglycémie au moment des prises alimentaires.
Une révolution sur l'appréhension du diabète de type 1
Ce nouveau médicament peut actuellement aider les personnes aux premiers stades de la maladie à gagner du temps : jusqu'à trois ans, avant de devenir dépendantes des injections d'insuline. La disponibilité de ce traitement pose désormais la question du dépistage chez les enfants : cette notion selon laquelle le dépistage serait une bonne idée a toujour existé mais les experts médicaux ne l'ont jamais vraiment mise en place dans le diabète de type 1 car très peu de personnes dépistées seront atteintes de cette maladie, qui ne touche que quatre personnes sur 1 000 dans la population générale, soit 1,4 million d'Américains.
Elle pose également celle de la définition du diabète de type 1, non plus seulement comme une maladie métabolique, mais comme une maladie immunologique qu'il serait possible de traiter avant même un trouble métabolique, c'est-à-dire avant la perte des cellules bêta en rapport avec le dédordre immunitaire. On n'en est pas encore là et, même si certains chercheurs veulent un essai à un stade plus précoce, avant tout trouble métabolique, on n'a aucune idée si cela marche : si un enfant a des anticorps mais que son pancréas n'est pas activement attaqué, le traitement peut ne pas être utile.
Le teplizumab peut changer la donne dans le diabète de type 1
"Pendant 100 ans, les personnes atteintes de diabète de type 1 ont compté sur l'insuline pour traiter la maladie, et la décision d'aujourd'hui signifie que pour la première fois, la cause fondamentale de la maladie - une attaque du système immunitaire - peut être combattue et le diabète de type 1 potentiellement retardé jusqu'à trois ans”, a déclaré dans le Daily Mail Chris Askew, le directeur général de Diabetes UK, qui met tout en oeuvre pour l’autorisation de mise sur le marché au Royaume-Uni.
La date de mise à disposition de ce médicament en France n’est pas encore connue.