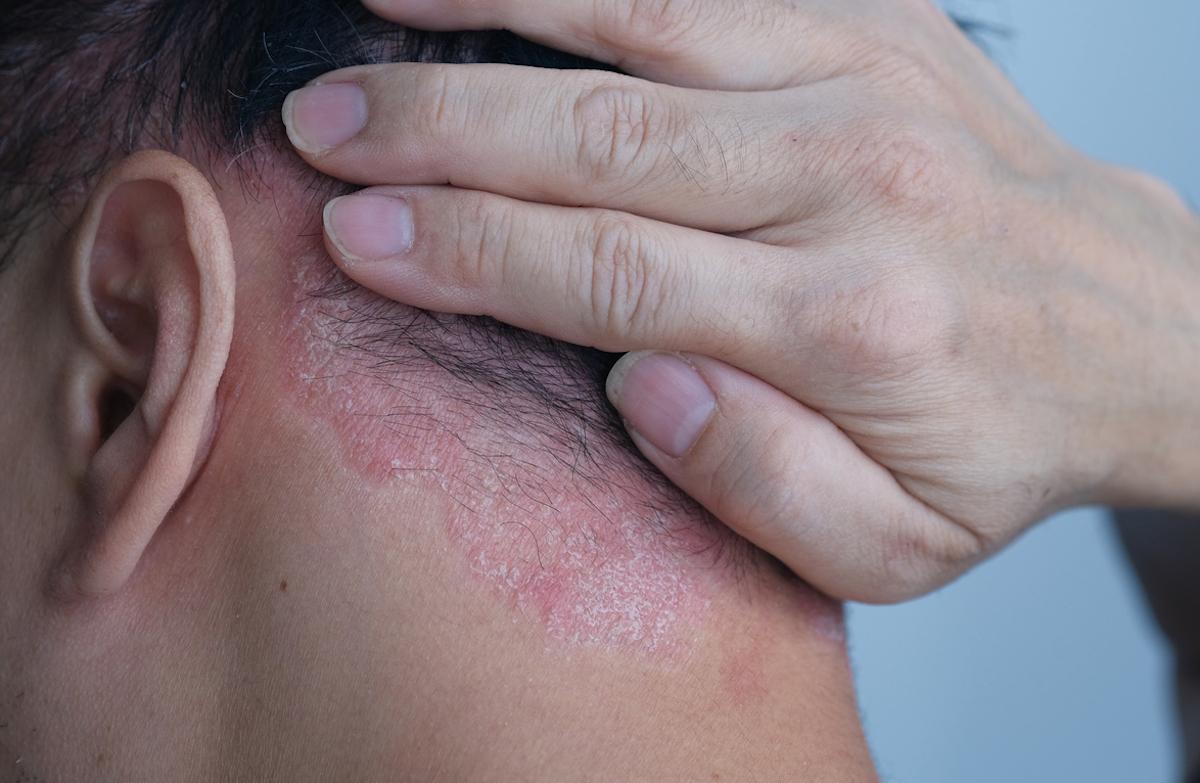
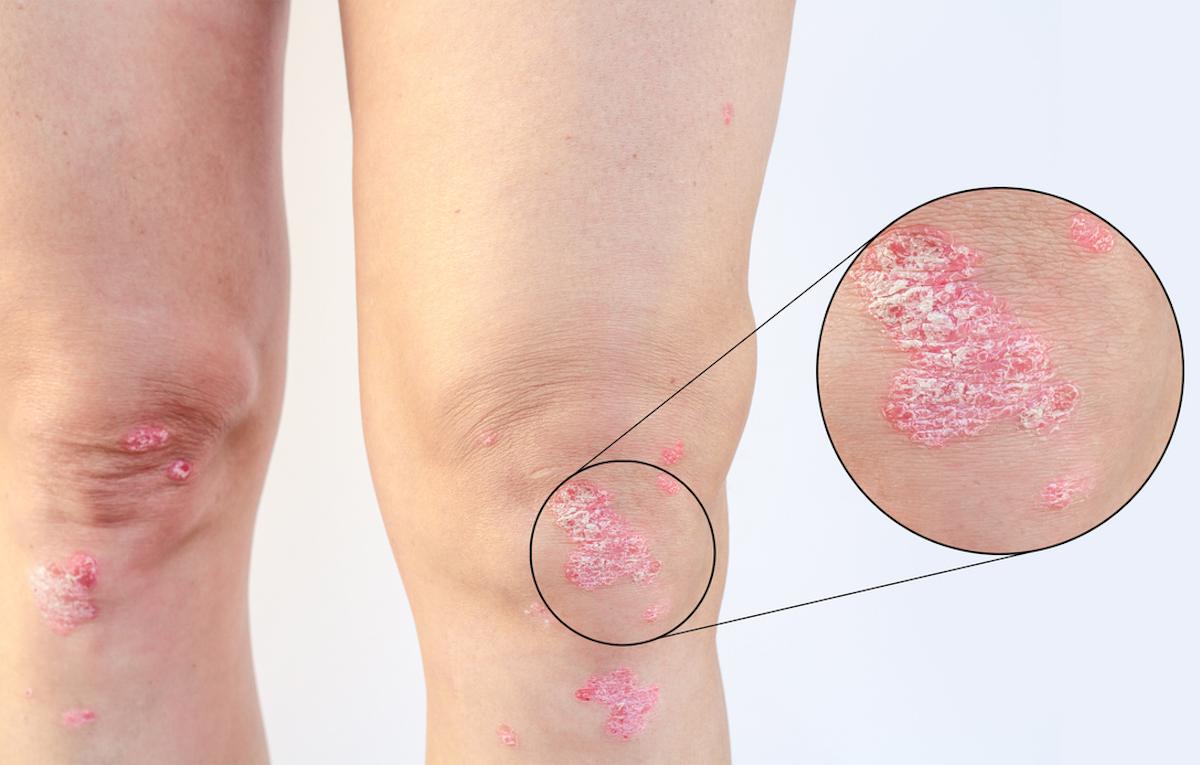
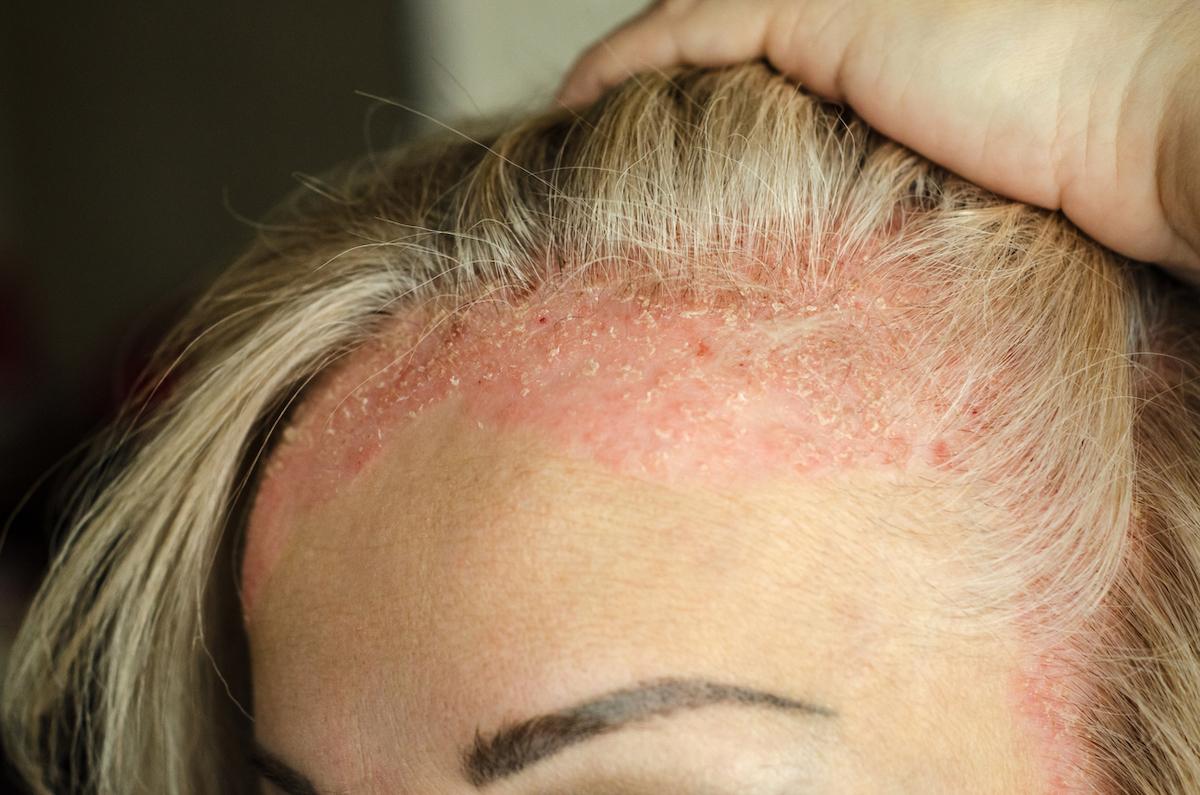
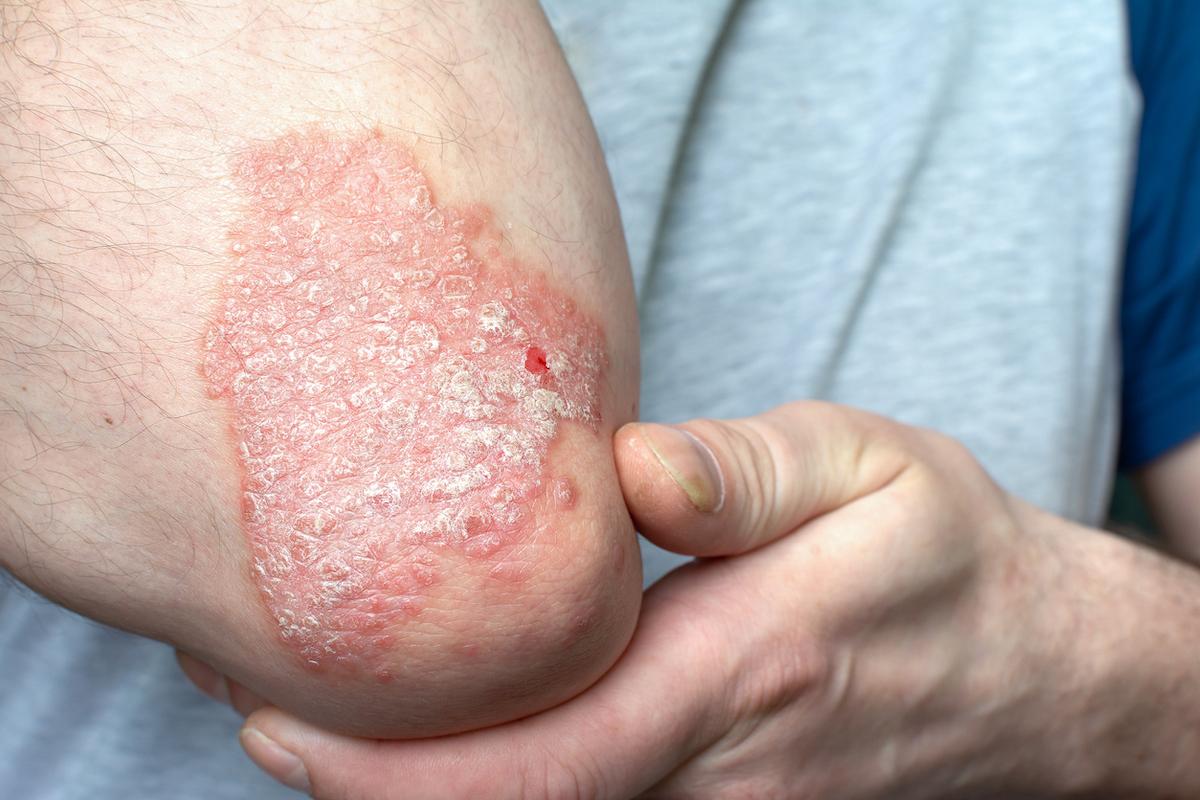
Dermatologie
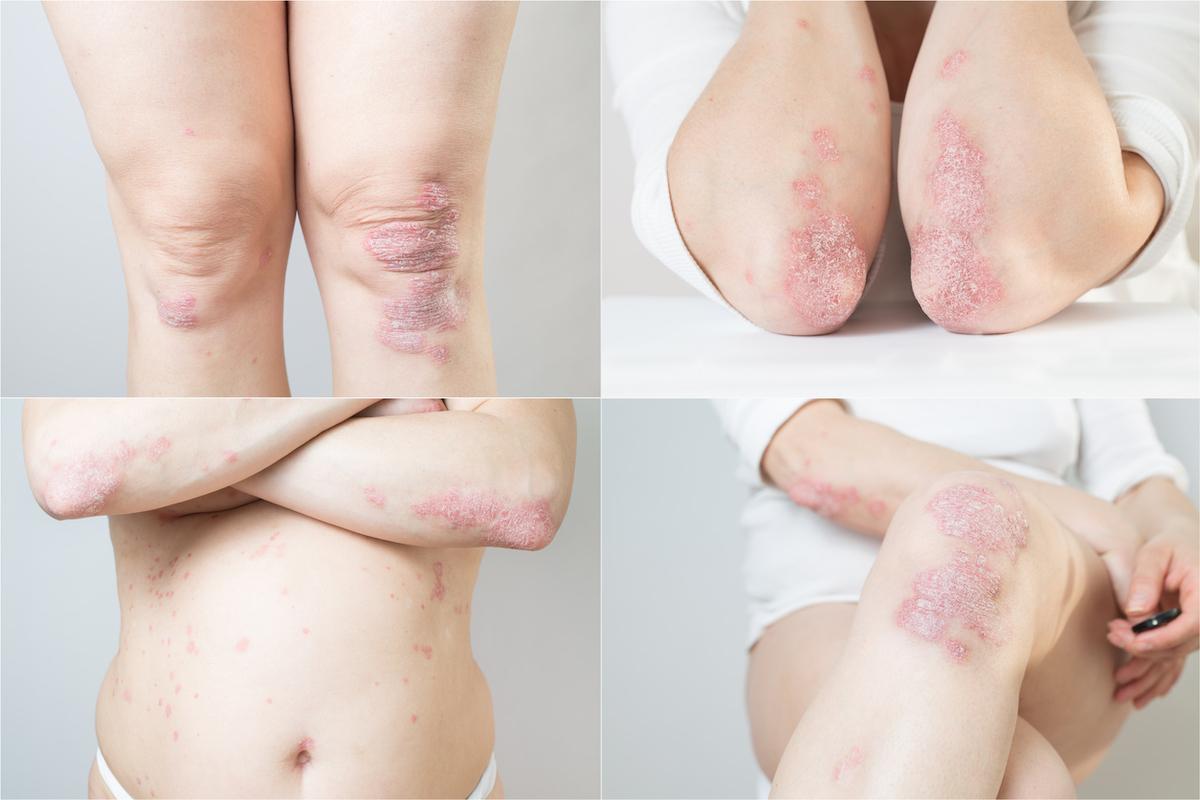
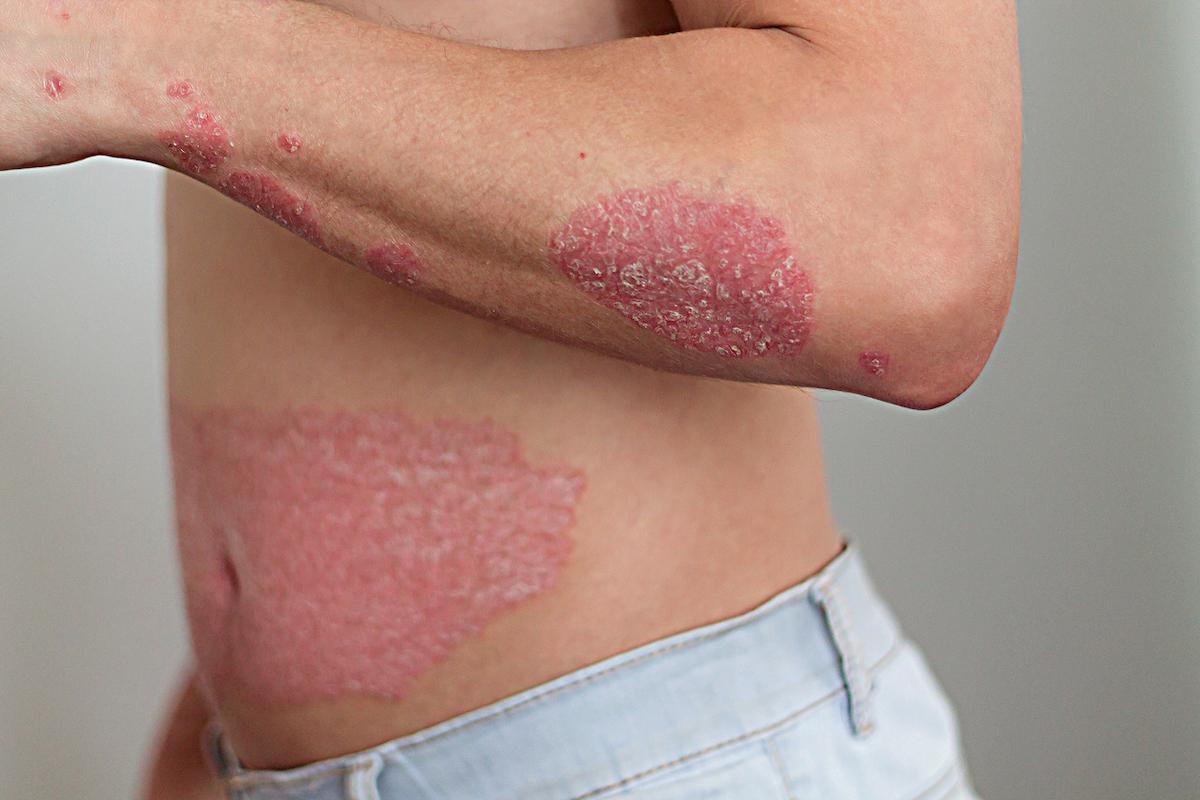
Psoriasis : un peptide oral anti-IL-23R biothérapie-like ?
L’icotrokinra, un peptide oral ciblant le récepteur de l’IL-23, obtient des taux de blanchiment cutané supérieurs au placebo et au traitement oral de référence, avec une tolérance proche du placebo.
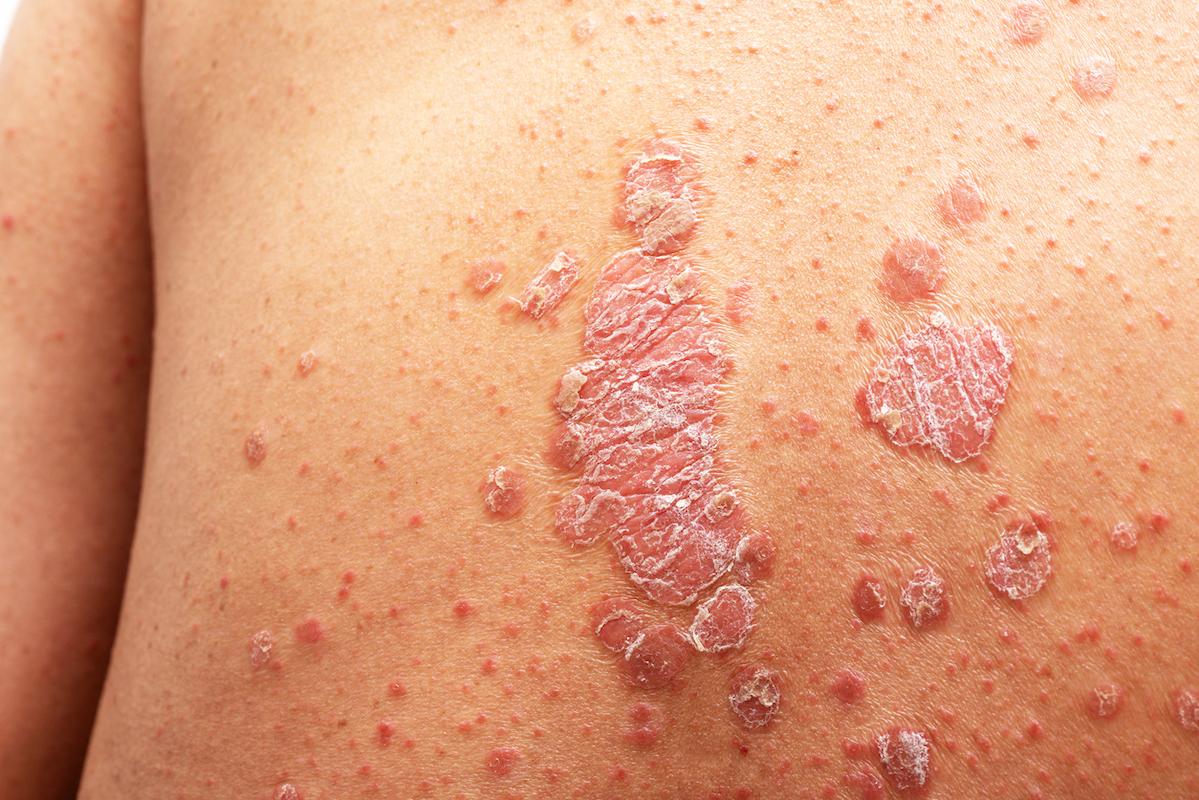
- tumeyes/istock
La prise en charge systémique du psoriasis modéré à sévère s’est transformée grâce aux anticorps anti-TNF, anti-IL17 et anti-IL-23/IL-12/23, au prix d’une administration parentérale. L’icotrokinra (JNJ-77242113) est un peptide oral qui se fixe sélectivement sur le récepteur de l’IL-23, bloquant son signal et l’activation T pathogène.
Dans deux essais de phase 3 parallèles, randomisés, en double insu, contrôlés versus placebo et comparateur actif (ICONIC-ADVANCE 1 et 2), des adultes atteints de psoriasis en plaques modéré à sévère ont reçu de l’icotrokinra 200 mg/j, un placebo ou le deucravacitinib 6 mg/j.
À 16 semaines, les co-critères étaient l’IGA 0/1 avec amélioration ≥2 grades et le PASI90. Tous ont été atteints : ADVANCE 1, IGA 0/1 68 % avec icotrokinra versus 11 % sous placebo (différence 58 %, p<0,0001), PASI90 55 % versus 4 % (différence 51 %, p<0,0001) ; ADVANCE 2, IGA 0/1 70 % versus 9 % (différence 62 %, p<0,0001), PASI90 57 % versus 1 % (différence 56 %, p<0,0001). Ces réponses, d’emblée élevées, se sont poursuivies jusqu’à la semaine 24. Ces résultats sont publiés dans The Lancet.
Un signal fort en faveur d’icotrokinra versus deucravacitinib
Au-delà des critères coprincipaux, l’icotrokinra surpasse le deucravacitinib, le traitement oral de référence, sur des objectifs de blanchiment complet : en semaine 16, PASI100 31 % vs 11 % et IGA 0 37 % vs 16 % dans ADVANCE 1 ; PASI100 32 % vs 14 % et IGA 0 37 % vs 17 % dans ADVANCE 2 (toutes comparaisons p<0,0001). Le bénéfice clinique s’accompagne d’une tolérance favorable.
À 16 semaines, les événements indésirables sont rapportés chez 48 % sous icotrokinra et 57 % sous placebo ; les événements indésirables les plus fréquents sont des problèmes ORL bénins (rhinopharyngite 6 % vs 5 %, infections des voies aériennes supérieures 4 % vs 3 %). À 24 semaines, la proportion de patients avec au moins un événement indésirable est plus faible avec l’icotrokinra qu’avec le deucravacitinib (57 % vs 65 %). Aucun signal de tolérance majeur n’a émergé au cours de ces analyses intermédiaires. L’ensemble soutient une efficacité « de type biologique » par voie orale, supérieure à l’option orale de référence (TYK2), tout en conservant un profil de tolérance comparable au placebo.
Un besoin d’alternative orale « ciblée »
Les essais ADVANCE 1 (149 centres, 13 pays) et ADVANCE 2 (114 centres, 11 pays) ont inclus 774 et 731 participants randomisés (schémas 2:1:2 et 4:1:4). Les patients sous placebo passaient à l’icotrokinra à S16 et ceux sous deucravacitinib à S24 ; l’analyse rapportée couvre 24 semaines d’études de 3 ans. La population, d’âge moyen 46,5 ans (≈80 % de sujets blancs, 68 % d’hommes), comportait 20 % de formes IGA=4 ; plus des deux tiers avaient reçu un traitement systémique antérieur, un quart une biothérapie. La robustesse méthodologique (double insu, contrôle actif, stratification par poids et région, effectifs élevés) renforce la validité externe, mais plusieurs limites appellent prudence : lecture à 24 semaines, switch programmé des bras placebo/actif, hétérogénéité géographique, et représentativité ethnique/sexuelle perfectible. Les données d’extension (durabilité, immunogénicité, infections opportunistes, MMG/MAE) seront déterminantes pour positionner icotrokinra face aux anti-IL-23 injectables.
Selon un éditorial associé, l’icotrokinra propose une option orale efficace pour les patients éligibles à une biothérapie mais réticents aux injections, ou pour lesquels la logistique du froid est un frein. Chez des malades nécessitant une réponse rapide et profonde (PASI90/100, IGA 0/1), les résultats plaident pour intégrer ce peptide anti-IL-23R dans l’algorithme avant de recourir aux biothérapies injectables, en particulier lorsque l’observance d’une prise quotidienne est jugée fiable.
Les perspectives incluent l’évaluation à 52 semaines et au-delà (persistance, rémission, stratégie d’entretien), l’exploration dans le rhumatisme psoriasique et les sites à fort impact, et des comparaisons face-face avec des anti-IL-23 p19 injectables. D’ici là, pour un psoriasis modéré à sévère, l’icotrokinra combine la précision immunologique des biothérapies anti-IL-23 et la commodité de la voie orale, élargissant concrètement le champ des traitements personnalisés.