Rhumatologie
Syndrome de Raynaud : avancées du traitement en 2023
Le syndrome de Raynaud peut se présenter sous deux formes principales : primaire et secondaire à des connectivites. La prise en charge de cette affection dépend de ce contexte et nécessite une compréhension approfondie des avancées récentes dans les domaines du diagnostic, de la génétique et du traitement.
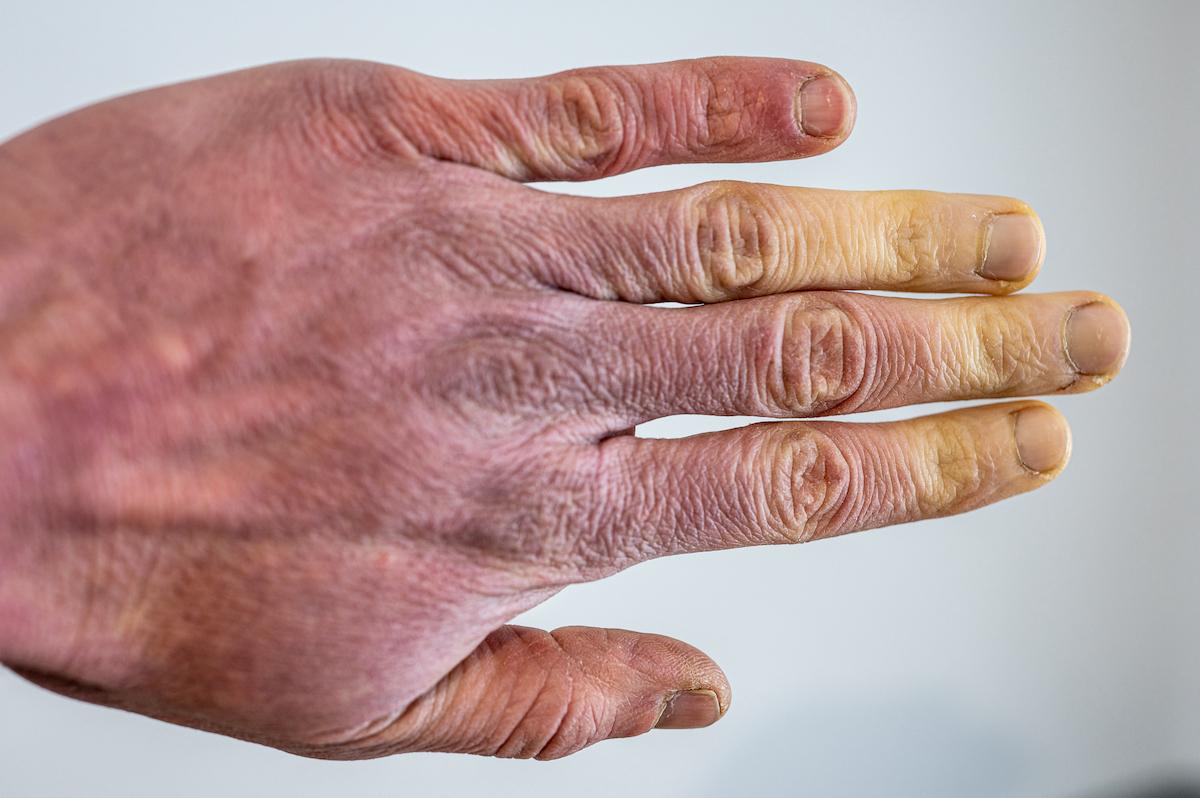
- SzymonBartosz/istock
Le phénomène de Raynaud est une affection fréquente car il toucherait 10 à 15% de la population française. Le syndrome de Raynaud peut se présenter sous deux formes principales : primaire et secondaire. Ces deux formes présentent des différences cliniques et physiopathologiques importantes. La plupart du temps il s’agit d’un syndrome de Raynaud primitif, sans pathologie sous-jacente, dont le traitement est plus simple que celui du syndrome de Raynaud secondaire à une connectivite.
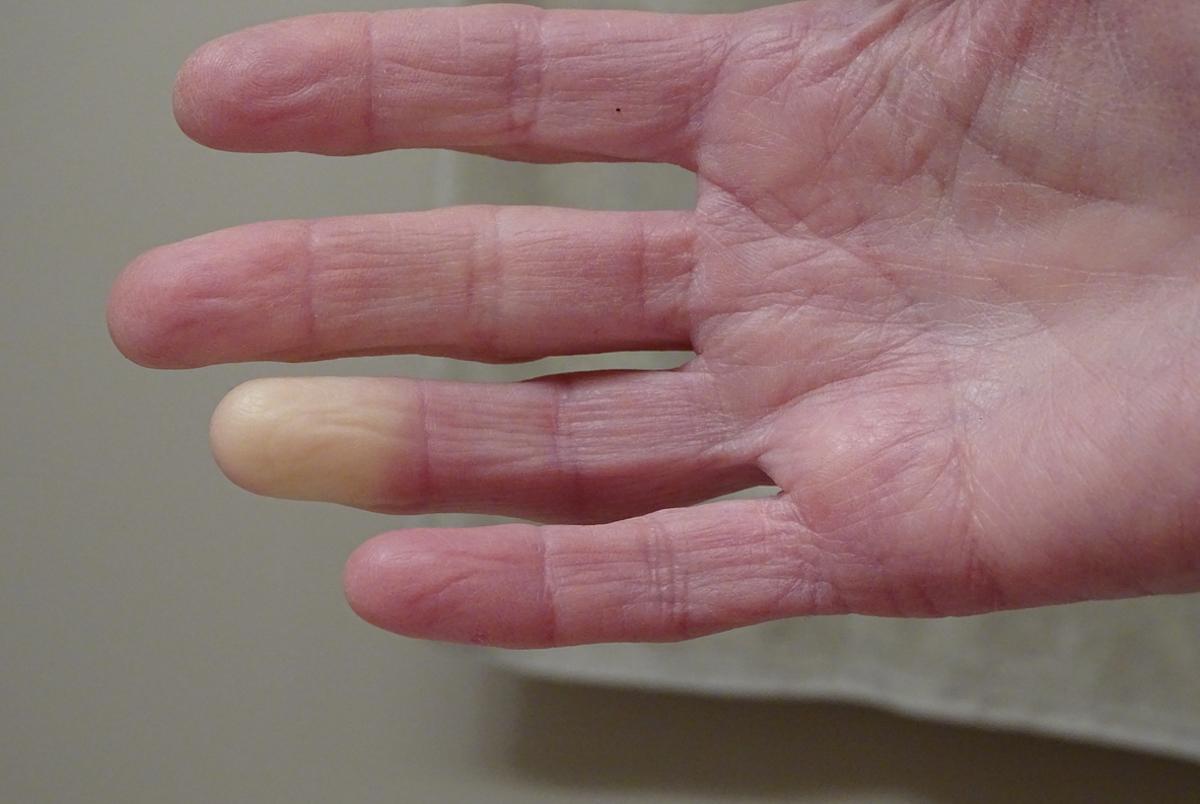
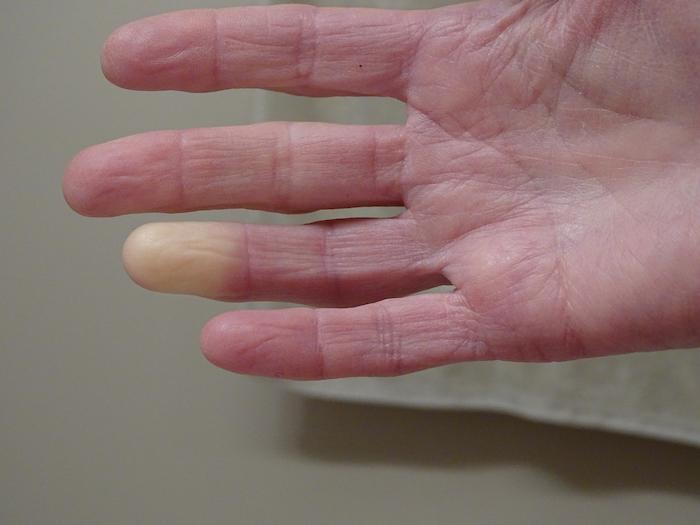
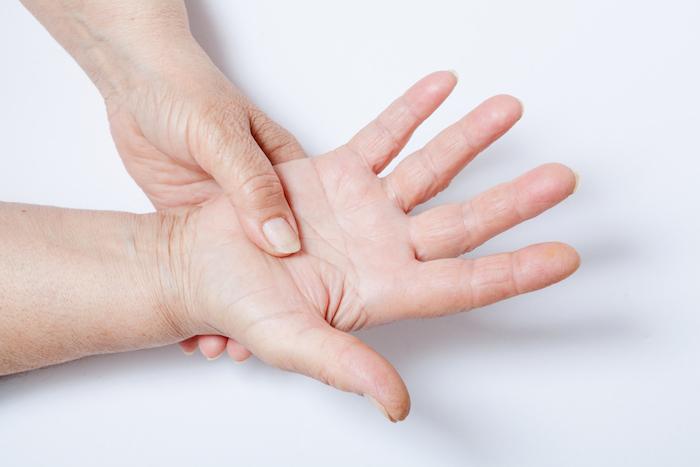
Le phénomène de Raynaud consiste en un trouble vaso-spastique qui se caractérise par une hypoperfusion digitale en réponse au froid ou à un stress émotionnel, engendrant douleur et handicap. La prise en charge de cette affection nécessite une compréhension approfondie des avancées récentes dans les domaines du diagnostic, de la génétique et du traitement.
Deux types de syndrome de Raynaud avec des traitements adaptés
Le syndrome de Raynaud primaire (ou maladie de Raynaud) est généralement bénin. Il se manifeste plutôt avant l'âge de 30 ans. Les épisodes de changement de couleur des doigts (blanchiment, cyanose, puis rougeur) sont généralement symétriques et sans ulcération ou gangrène. Il n'est pas associé à une maladie sous-jacente. Le mécanisme exact reste mal compris, mais il semble impliquer une hypersensibilité des récepteurs vasculaires au froid et au stress, conduisant à une vasoconstriction excessive. Il n'y a pas de dommage structurel significatif des vaisseaux sanguins.
Le syndrome de Raynaud secondaire est associé à une maladie sous-jacente, souvent une connectivite comme une sclérodermie, un syndrome de Sharp (connectivite mixte) ou une dermatomyosite, mais aussi un lupus érythémateux systémique, une polyarthrite rhumatoïde. Cette forme secondaire apparaît donc généralement après l'âge de 30 ans. Les symptômes peuvent être asymétriques et plus sévères, avec un risque accru d'ulcération des doigts, de cicatrisation lente, et de gangrène. D'autres symptômes de la connectivite sous-jacente sont souvent associés. La pathophysiologie est liée à la maladie sous-jacente. Dans le cas de la sclérodermie, par exemple, il y a une fibrose et un remodelage des vaisseaux sanguins, entraînant une diminution du flux sanguin. Des auto-anticorps spécifiques peuvent être présents, et des altérations immunitaires jouent souvent un rôle. La capillaroscopie du lit de l'ongle peut révéler des anomalies spécifiques, comme des mégacapillaires ou des zones « d'avascularité ».
En pratique, la distinction entre le syndrome de Raynaud primaire et secondaire est cruciale car elle a des implications importantes pour le diagnostic, le traitement et le pronostic. Le Raynaud primitif a tendance à être moins sévère et sans maladie sous-jacente, tandis que le Raynaud secondaire est souvent plus grave et associé à d'autres maladies systémiques.
Génétique du syndrome de Raynaud
Des études récentes ont révélé que, malgré une héritabilité élevée rapportée, aucun gène causal n'avait été robustement identifié pour la maladie de Raynaud. Toutefois, une étude d'association pangénomique incluant 5 147 cas de phénomène de Raynaud (RP) et 439 294 témoins a identifié trois nouvelles régions génomiques associées au risque de Raynaud primitif.
Parmi celles-ci, les gènes ADRA2A et IRX1 ont été priorisés comme candidats causaux. Cette découverte met en lumière le rôle potentiel de la signalisation des récepteurs adrénergiques α2A, codée par ADRA2A, dans la sensibilité aux vasospasmes induits par les catécholamines.
Des scores pour évaluer la gravité du Raynaud
L'ajustement optimal du traitement du syndrome de Raynaud nécessite une évaluation de la gravité qui peut s’appuyer sur plusieurs scores et outils de mesure, conçus pour évaluer la fréquence, la durée, l'intensité des symptômes et l'impact sur la qualité de vie :
• Échelles Visuelles Analogiques (EVA) : ces échelles permettent aux patients de noter leur douleur ou l'inconfort sur une ligne graduée, offrant une mesure subjective mais simple et utile de l'intensité des symptômes.
• Raynaud's Condition Score (RCS) : le RCS est un outil d'auto-évaluation où les patients notent la sévérité de leurs symptômes sur une échelle. Il prend en compte des facteurs comme la couleur, la douleur, la fonctionnalité et la durée des épisodes.
• Raynaud's Severity Score : ce score est basé sur l'évaluation de la fréquence et de la sévérité des attaques. Il peut inclure des mesures telles que le nombre d'attaques par jour ou par semaine et leur impact sur les activités quotidiennes.
• Digital Ulcer Severity Score : ce score est utilisé spécifiquement pour évaluer la sévérité des ulcères digitaux, un problème courant dans les cas graves de Raynaud, en particulier dans le Raynaud secondaire.
• Capillaroscopie du lit de l'ongle : bien qu'elle ne soit pas un score à proprement parler, la capillaroscopie est un outil diagnostique important pour évaluer les changements microvasculaires associés au syndrome de Raynaud, en particulier dans le contexte de maladies systémiques comme la sclérodermie.
• Health Assessment Questionnaire (HAQ) : Bien qu'utilisé principalement pour les maladies rhumatologiques, le HAQ peut être adapté pour évaluer l'impact du syndrome de Raynaud sur la qualité de vie, en particulier la capacité à réaliser des tâches quotidiennes.
• Questionnaires de qualité de vie : Des outils comme le Short Form (36) Health Survey (SF-36) peuvent être utilisés pour évaluer l'impact global du syndrome de Raynaud sur le bien-être et la qualité de vie du patient.
Ces scores et outils aident les prescripteurs à évaluer l'efficacité des traitements et à adapter la prise en charge en fonction de la progression de la maladie et de la réponse du patient. Ils sont particulièrement importants dans les cas de Raynaud secondaire, où le suivi de la sévérité peut fournir des informations cruciales sur la maladie sous-jacente.
Un panel de traitements variés dans le Raynaud primitif et secondaire
Le traitement du syndrome de Raynaud, qu'il soit primitif ou secondaire, vise à réduire la fréquence et la sévérité des épisodes vasospastiques, mais les approches peuvent différer selon qu'il s'agit d'une forme primitive ou secondaire de la maladie. Il commence toujours par des mesures non pharmacologiques, comme éviter l'exposition au froid, arrêter de fumer, et gérer le stress. Les modifications du mode de vie, comme l'éviction du tabac, la gestion du stress et la protection contre le froid, sont également importantes.
Il est important que les médecins individualisent le traitement pharmacologique pour chaque patient, en tenant compte de la tolérance du médicament et des besoins spécifiques du patient. La collaboration étroite entre le patient et le médecin est cruciale pour optimiser le traitement du syndrome de Raynaud.
À la base du traitement pharmacologique du syndrome de Raynaud, les bloqueurs des canaux calciques (BCC), ou inhibiteurs calciques, jouent un rôle central. Ils sont souvent le premier choix de traitement en raison de leur efficacité à réduire les spasmes des vaisseaux sanguins et à améliorer le flux sanguin. La nifédipine est probablement l’inhibiteur calcique le plus fréquemment prescrit pour le syndrome de Raynaud. La nifédipine agit en relaxant les muscles lisses des vaisseaux sanguins, ce qui augmente le flux sanguin vers les extrémités. L’amlodipine est souvent choisie pour son efficacité et son profil d'effets secondaires relativement favorable. La felodipine et l’isradipine sont similaires à l'amlodipine et peuvent être utilisés chez les patients qui ne tolèrent pas les autres inhibiteurs calciques ou en cas de contre-indications. Le diltiazem est moins couramment utilisé pour le syndrome de Raynaud que les autres inhibiteurs calciques. Les inhibiteurs calciques sont généralement bien tolérés, mais peuvent avoir des effets secondaires tels que des maux de tête, des bouffées vasomotrices, des étourdissements, et parfois des œdèmes. Le choix du médicament spécifique et sa posologie dépendent de plusieurs facteurs, notamment la gravité des symptômes, la présence d'autres maladies associées et la réponse individuelle au traitement.
Si un patient atteint du syndrome de Raynaud ne répond pas de manière adéquate aux inhibiteurs calciques, plusieurs autres options de traitement peuvent être envisagées :
• Inhibiteurs de la phosphodiestérase 5 (PDE5i) : les inhibiteurs de la phosphodiestérase 5 (PDE5i) représentent une classe de médicaments prometteuse pour le traitement de la maladie de Raynaud. Ils augmentent le flux sanguin vers les extrémités et peuvent ainsi réduire la fréquence et la durée des attaques de Raynaud primitif. Les études ont montré que les PDE5i, comme le tadalafil, le sildenafil et le vardenafil, réduisent en moyenne de trois attaques par semaine la fréquence des attaques de Raynaud primitif (sur une vintaine !) et diminuent la durée des attaques de cinq minutes en moyenne. Cependant, ces bénéfices doivent être mis en balance avec les effets indésirables potentiels, qui peuvent inclure un taux plus élevé d'abandon du traitement.
• Antagonistes des récepteurs de l'Endothéline : des médicaments comme le bosentan peuvent être utilisés, surtout dans les cas de Raynaud secondaire associé à des maladies systémiques comme la sclérodermie.
• Prostaglandines : dans les cas sévères, notamment avec des ulcères digitaux ou des menaces de gangrène, les prostaglandines telles que l’iloprost peuvent être administrées par voie intraveineuse. Elles sont efficaces pour améliorer la circulation sanguine périphérique, y compris sur le long terme.
• Antidépresseurs : les antidépresseurs, en particulier ceux qui agissent sur la sérotonine comme les inhibiteurs sélectifs de la recapture de la sérotonine (ISRS), peuvent être bénéfiques dans certains cas.
• Agents sympatholytiques : des médicaments comme la prazosine, qui bloquent certains récepteurs adrénergiques, peuvent être utilisés pour diminuer la vasoconstriction.
• Traitements non pharmacologiques : des mesures telles que la biofeedback, l'acupuncture et l'exercice peuvent aider certains patients. Les modifications du mode de vie, comme l'éviction du tabac, la gestion du stress et la protection contre le froid, sont également importantes.
• Chirurgie : dans les cas extrêmes, notamment lorsque d'autres traitements ont échoué et que le patient souffre de complications graves, des procédures chirurgicales comme la sympathectomie digitale peuvent être envisagées.
Un traitement différencié entre Raynaud primitif et secondaire
Le traitement du syndrome de Raynaud Primaire commence généralement par des mesures non pharmacologiques, comme éviter l'exposition au froid, arrêter de fumer, et gérer le stress. Ces mesures sont souvent suffisantes pour les personnes atteintes d’une forme bénigne.
Si nécessaire, les médicaments utilisés incluent principalement les inhibiteurs calciques, qui aident à dilater les vaisseaux sanguins et à améliorer la circulation. Les interventions médicamenteuses dans la forme primitives sont généralement moins agressives, et l'utilisation de médicaments plus puissants est rare, sauf si les symptômes sont particulièrement sévères.
Le traitement du syndrome de Raynaud Secondaire repose avant tout sur le traitement de la maladie sous-jacente et sur une approche pharmacologique plus intensive : il est ainsi crucial de traiter la maladie sous-jacente, comme une sclérodermie ou le lupus, car cela peut directement affecter la gravité des symptômes de Raynaud, en particulier la fiibrose.
En plus des bloqueurs des canaux calciques, l’association d’autres médicaments peut être nécessaires pour gérer les symptômes, notamment les inhibiteurs de la PDE5, les antagonistes des récepteurs de l'endothéline, et parfois les prostaglandines.
Les patients atteints de la forme secondaire du syndrome de Raynaud doivent être surveillés de près pour détecter les signes de complications, comme les ulcères digitaux ou les infections, qui peuvent nécessiter des traitements spécifiques, y compris parfois la chirurgie.
Le traitement du Raynaud secondaire peut impliquer une équipe de spécialistes, y compris des rhumatologues, des dermatologues et des spécialistes des maladies vasculaires, pour gérer à la fois le Raynaud et la maladie sous-jacente.
En résumé, bien que les principes de base du traitement du syndrome de Raynaud restent similaires dans les deux formes mais le traitement du Raynaud secondaire est souvent plus complexe et nécessite une gestion plus approfondie de la maladie sous-jacente ainsi qu'une surveillance plus étroite pour les complications.
Gestion pratique et stratégies thérapeutiques
En termes de gestion pratique, il est essentiel d'évaluer le risque de progression vers la sclérodermie systémique (SSc) chez les patients atteints de Raynaud primitifs atypiques, en utilisant des outils comme les autoanticorps et la capillaroscopie du lit de l'ongle. Les bloqueurs des canaux calciques sont le traitement de première ligne et peuvent être initiés par les médecins de premier recours.
Pour les cas réfractaires, des traitement médicamenteux de deuxième ligne sont disponibles, et l'intervention chirurgicale peut également être envisagée. Les stratégies de traitement varient considérablement à l'international, soulignant l'importance d'une approche personnalisée dans la prise en charge de la maladie de Raynaud.
Conclusion
La prise en charge du syndrome de Raynaud en 2023 s'appuie sur des avancées significatives dans la compréhension de sa génétique et l'amélioration des options thérapeutiques. L'identification des gènes ADRA2A et IRX1 offre de nouvelles perspectives pour comprendre et traiter cette affection. Parallèlement, l'utilisation des inhibiteurs PDE5i apporte une amélioration notable dans la gestion des symptômes, bien que leur utilisation doive être soigneusement équilibrée avec la surveillance des effets indésirables. Enfin, une approche pratique et mise à jour de l'évaluation et de la gestion des patients atteints de Raynaud Primitif, incluant des conseils sur l'initiation et l'escalade des médicaments, est essentielle pour offrir les meilleurs soins possibles.