Onco-dermatologie
Mélanome à risque : l'immunothérapie néoadjuvante change le pronostic
Dans le mélanome de stade III-IV considéré comme résécable, commencer le pembrolizumab en néoadjuvant, avant la chirurgie de résection, au lieu d'attendre après, améliore la survie sans évènement.
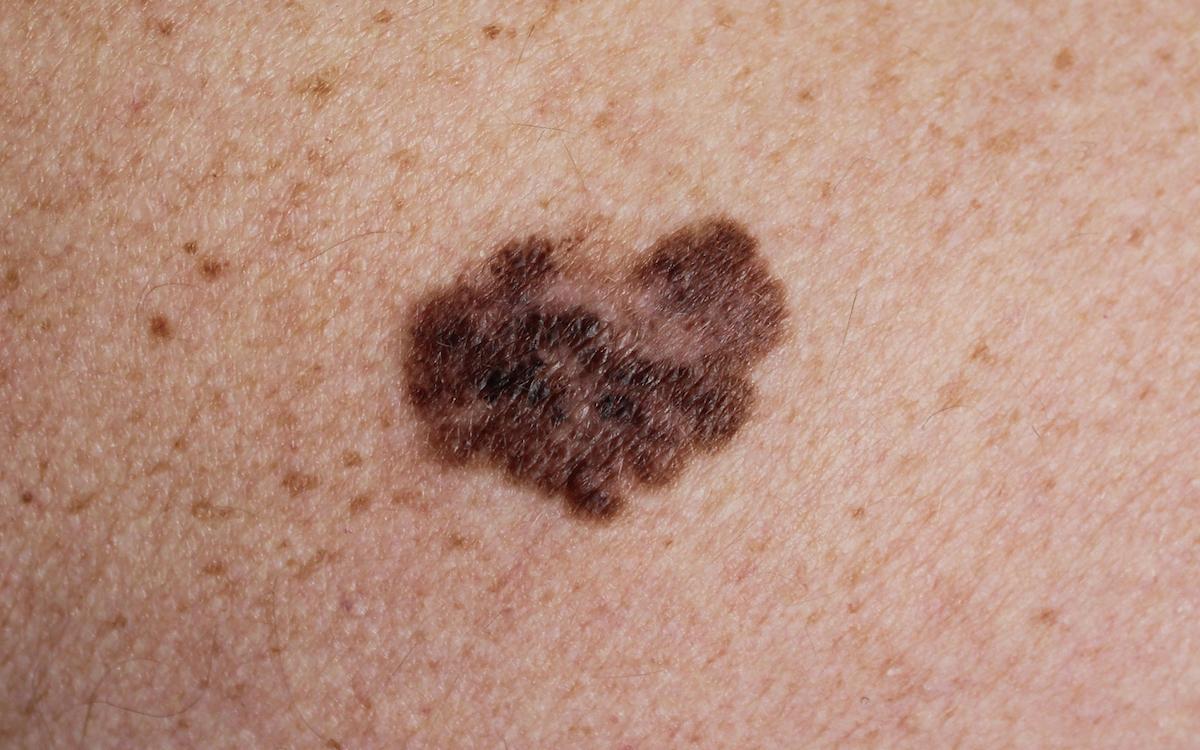
- Nasekom/istock
Les patients atteints d'un mélanome à haut risque qui ont reçu l'immunothérapie par pembrolizumab en néoadjuvant et en adjuvant ont un risque significativement plus faible de récidive de leur cancer que les patients similaires ayant reçu le médicament uniquement en adjuvant : le taux d'événements est inférieur de 42% chez les patients recevant le régime néoadjuvant.
Ces résultats sont issus de l’étude S1801, menée par le SWOG Cancer Research Network, un groupe de recherche sur le cancer financé par le National Cancer Institute (NCI) aux États-Unis, ont été présentés lors du Congrès 2022 de la Société européenne d'oncologie médicale (ESMO) (abstract LBA6).
Amélioration de la survie sans évènement
Le critère principal mesuré était la durée de survie sans événement, définie comme le temps écoulé entre la randomisation et la survenue de l'un des éléments suivants : progression de la maladie ou toxicité ayant entraîné l'absence de chirurgie, absence de début de traitement adjuvant dans les 84 jours suivant la chirurgie, récidive du mélanome après la chirurgie ou décès toutes causes confondues.
Avec un suivi médian de 14,7 mois, la survie sans événement est significativement plus longue dans le groupe recevant le traitement néoadjuvant, avec un rapport de risque de 0,58 par rapport au groupe recevant le traitement adjuvant, ce qui correspond à un taux d'événements inférieur de 42% chez les patients recevant le régime néoadjuvant.
Plus d’évènements après le traitement dans le groupe adjuvant
Le bénéfice du traitement néoadjuvant est cohérent dans toute une série de sous-groupes, notamment en fonction de l'âge, du sexe, de l'état de performance, du statut BRAF et du stade de la maladie. Ils ont également constaté que les taux d'événements indésirables (effets secondaires) sont similaires dans les deux bras de l'étude et que le pembrolizumab néoadjuvant n'entraîne pas d'augmentation des événements indésirables liés à la chirurgie.
Surtout, un nombre similaire de patients dans les deux bras ont eu des événements avant d'initier le pembrolizumab en adjuvant, mais que le taux d'événements après l'initiation du traitement adjuvant est plus élevé dans le bras adjuvant.
Meilleure mémoire immunologique
Le mécanisme d'action des anti-PD1/PDL1, tels que le pembrolizumab, est souvent décrit comme une levée du frein à la réponse du système immunitaire vis-à-vis des cellules tumorales. Les chercheurs de l'étude S1801 ont émis l'hypothèse qu'il y aurait une réponse immunitaire antitumorale plus importante et une mémoire immunologique plus longue si le pembrolizumab était administré alors que la tumeur du mélanome était encore présente, plutôt qu'après l'ablation, lorsque le système immunitaire répondrait principalement aux cellules cancéreuses micrométastatiques.
Pour tester cette hypothèse, les investigateurs de l'étude S1801 ont recruté 345 participants avec un mélanome de stade IIIB à IV jugé opérable. Les participants âgés de 18 à 90 ans ont été randomisés pour recevoir, soit une chirurgie initiale suivie de 200 mg de pembrolizumab toutes les trois semaines (traitement adjuvant) pour un total de 18 doses, soit 200 mg de pembrolizumab toutes les trois semaines pour trois doses précédant la chirurgie (traitement néoadjuvant), puis 15 doses supplémentaires après la chirurgie (traitement adjuvant).
En pratique
Le traitement néoadjuvant n’a absolument pas compromis les résultats de la chirurgie. Sous réserve d’une confirmation des résultats à plus long terme, l'étude S1801 est nettement en faveur de l’immunothérapie néoadjuvante afin de générer une réponse immunitaire pendant que la majeure partie du mélanome et les cellules T antitumorales sont intactes.
Il reste à déterminer quelle est l’intensité et la durée optimales du traitement néoadjuvant, éventuellement afin de réduire l’importance de la chirurgie. Le traitement néoadjuvant pourrait également aider à identifier chirurgicalement les patients qui répondront bien aux anti-PD1/PDL1 et permettre ainsi une meilleure adaptation thérapeutique.