Dermatologie
Carcinome épidermoïde cutané : l'interleukine 2, une alternative à la chirurgie
L'IL-2 peut -etre considérée comme une option thérapeutique à part entière chez les patients porteurs d'un CEC non opérable, multirécidivant ou localisé dans une zone fonctionnellement ou esthétiquement critique. Son coût nettement inférieur à celui des immunothérapies systémiques et sa facilité d'administration en font une option potentiellement pertinente
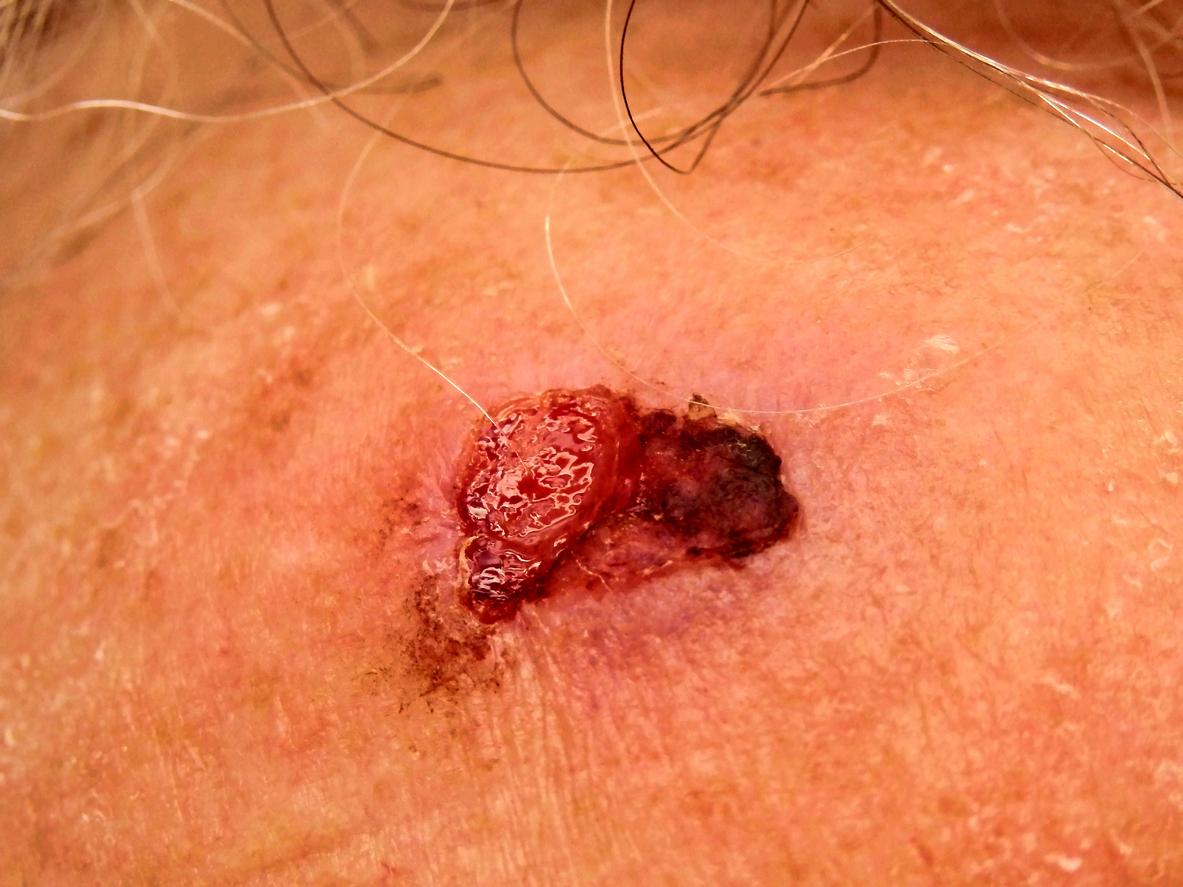
- PlazacCameraman/iSTOCK
Le carcinome épidermoïde cutané (CEC) représente l'une des tumeurs malignes les plus fréquentes dans la population générale. Si la résection chirurgicale demeure le traitement de référence, la prise en charge de formes récidivantes, localement avancées ou localisées dans des zones anatomiques sensibles reste un défi thérapeutique majeur, particulièrement chez des patients âgés et polypathologiques pour lesquels le risque opératoire peut être prohibitif. Dans ce contexte, une étude publiée en mars 2026 dans JAMA Dermatology lien apporte des données intéressantes sur l'utilisation de l'interleukine-2 administrée par voie intralésionnelle (IL-2) dans le traitement du CEC.
L'interleukine-2 est historiquement connue comme la première cytokine à avoir démontré une efficacité antitumorale chez l'homme. Son usage systémique a cependant rapidement été limité par des effets indésirables graves, notamment le syndrome de fuite capillaire et la tempête cytokinique. Pour contourner cette toxicité, une approche intralésionnelle a été développée et intégrée dans la pratique clinique canadienne dans le traitement du mélanome cutané métastatique, avec des taux de réponse globale supérieurs à 90 % et une quasi-absence d'effets de grade 3 ou 4. Fort de cette expérience, et en s'appuyant sur la relation bien établie entre immunosuppression ciblant l'IL-2 et risque accru de CEC (les transplantés d'organes présentent une incidence jusqu'à 250 fois supérieure à celle de la population générale), l'équipe de chirurgie oncologique de l'université Dalhousie à Halifax, au Canada, a étendu cette approche au traitement du CEC.
La série rapportée par Giacomantonio et collaborateurs porte sur 16 patients traités entre 2017 et 2024 dans un centre de référence unique. L'âge moyen était de 79 ans (extrêmes : 59-99 ans), avec une majorité d'hommes (9 sur 16). Les lésions concernaient principalement la région cervico-faciale (9 patients), ainsi que les membres inférieurs (3 patients) et une zone péri-anale (2 patients). Tous les patients présentaient un CEC invasif histologiquement confirmé, sans invasion périneurale. Ils avaient soit échoué à une ou plusieurs tentatives chirurgicales antérieures, soit présentaient des comorbidités contra-indiquant l'intervention, soit encore étaient porteurs de lésions en zone anatomiquement sensible pour lesquelles l'immunothérapie intralésionnelle a été proposée en alternative à la chirurgie mutilante.
Le protocole thérapeutique consistait en des injections intralésionnelles bihebdomadaires d'IL-2 à une concentration de 500 000 UI/0,1 mL, avec une dose ajustée à 0,1 mL par 2 mm2 de lésion cliniquement positive, jusqu'à un maximum de 20 millions d'UI par séance. Les lésions volumineuses étaient préalablement anesthésiées par infiltration de xylocaïne adrénalinée afin d'améliorer la tolérance des injections. La réponse clinique était évaluée en consultation par examen direct, photographie sériée et, si nécessaire, biopsie de contrôle, selon les critères iRECIST. Le traitement était poursuivi tant que le patient répondait et interrompu en cas de progression.
13 sur 16 patients ont obtenu une réponse complète
Les résultats sont notables. Sur les 16 patients, 13 ont obtenu une réponse complète, soit un taux de réponse complète de 81 %. Aucune réponse partielle n'a été enregistrée, faisant de ce taux de réponse complète également le taux de réponse global. La survie sans progression médiane s'établissait à 19 mois, avec des extrêmes allant de 1 à 77 mois, témoignant de la durabilité des réponses chez certains patients. Le nombre moyen de séances d'injection était de 10 (entre 2 et 32 selon les patients), pour une durée de traitement moyenne de 13 mois. Deux patients présentant des lésions métachrones multiples ont nécessité un traitement au long cours, toutes leurs lésions traitées répondant complètement à l'iIL-2 sans développement de résistance au fil du temps. Les trois patients non répondeurs ont bénéficié d'une chirurgie de rattrapage ou d'une chimiothérapie palliative.
Aucun effet indésirable de grade III ou supérieur
Sur le plan de la tolérance, les auteurs soulignent l'excellent profil de sécurité observé. Aucun patient n'a présenté d'effet indésirable de grade 3 ou supérieur. Les effets rapportés se limitaient à des symptômes pseudo-grippaux (fièvre, frissons, myalgies, malaise général) de grade 1, apparaissant dans les six à huit heures suivant l'injection et se résolvant spontanément en moins de vingt-quatre heures. Quelques patients ont signalé des nausées et un épisode de vomissements. Un cas de lichen plan cutané de grade 2 au site d'injection a également été noté. L'anesthésie locale préalable a significativement amélioré le confort procédural sans sembler affecter l'efficacité du traitement.
Mis en perspective avec les données disponibles pour d'autres options thérapeutiques, ces résultats méritent attention. Dans une étude multicentrique non randomisée récente portant sur 79 patients atteints de CEC opérable de stade II à IV, le cémiplimab en situation néoadjuvante avait permis d'obtenir une réponse complète chez 53 % des patients, avec une réponse partielle chez 13 % supplémentaires, mais au prix d'effets indésirables de grade 3 ou plus chez 18 % des participants. La série présentée ici, bien que portant sur un nombre plus limité de patients atteints de CEC de stade I à II, affiche un taux de réponse complète supérieur, dans une population particulièrement vulnérable, sans aucun effet sévère.
Les auteurs reconnaissent les limites inhérentes à ce travail : il s'agit d'une série de cas monocentrique, non randomisée, avec un risque de surestimation des taux de réponse. L'absence de bras comparateur et le faible effectif ne permettent pas de conclusions définitives. Ils plaident néanmoins pour que l'iIL-2 soit considérée comme une option thérapeutique à part entière chez les patients porteurs d'un CEC non opérable, multirécidivant ou localisé dans une zone fonctionnellement ou esthétiquement critique. Son coût nettement inférieur à celui des immunothérapies systémiques et sa facilité d'administration en font également une option potentiellement pertinente dans des contextes aux ressources limitées. Des essais randomisés restent nécessaires pour confirmer et préciser ces données préliminaires mais encourageantes.