Onco-Sein
Cancer du sein HER2+ : une désescalade de la chimiothéraie néoadjuvante guidée par IRM ?
L’étude TRAIN-3 montre qu’une stratégie de réduction de la chimiothérapie néoadjuvante guidée par IRM chez les patientes atteintes d’un cancer du sein HER2+ permet de maintenir des données de survie excellentes tout en diminuant la toxicité.
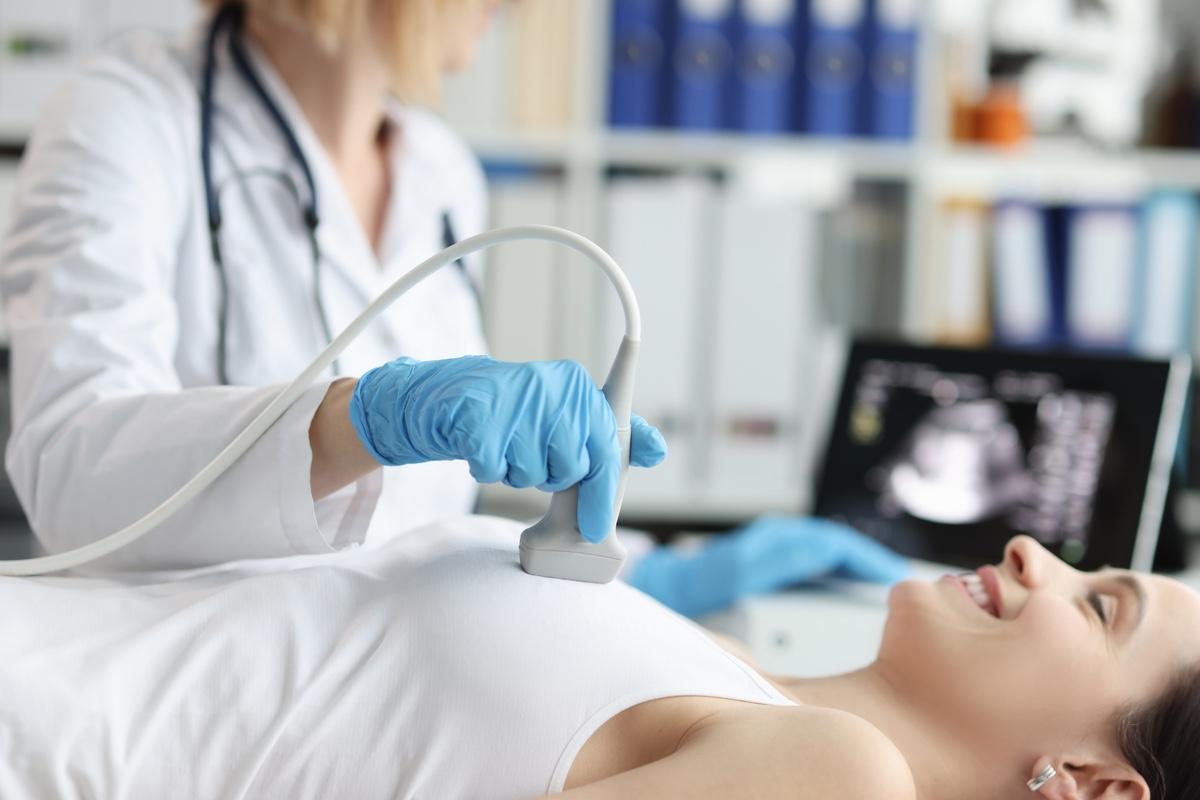
- SeventyFour/iStock
Le traitement standard des cancers du sein HER2+ de stade précoce repose habituellement sur six à neuf cycles de chimiothérapie associés à une thérapie anti-HER2, permettant d’obtenir des taux élevés de réponse pathologique complète et d’excellents résultats de survie (84 % à 98 % de survie sans événement à 3 ans), au prix néanmoins d’une toxicité notable et d’un impact significatif sur la qualité de vie.
Certaines patientes présentent cependant une réponse pathologique complète précoce après un à trois cycles seulement, suggérant qu’une poursuite systématique du traitement pourrait exposer à des toxicités évitables. L’objectif principal de TRAIN-3 est donc d’évaluer si l’IRM mammaire peut guider de manière sûre la réduction du nombre de cycles chez les patientes présentant une réponse radiologique complète rapide.
Des résultats préliminaires avaient montré qu’une réponse complète radiologique prédisait une réponse pathologique complète chez 87 % des patientes RH− et 53 % des patientes RH+. Sont rapportés dans cet article les résultats de survie sans événement à trois ans.
Une désescalade thérapeutique guidée par l’IRM
Cette étude multicentrique néerlandaise de phase II, à bras unique, a inclus 467 patientes atteintes d’un cancer du sein HER2+ de stade II-III (235 tumeurs RH− et 232 RH+). Au total, 87 % des tumeurs étaient classées T2-T3, 60 % présentaient une atteinte ganglionnaire, 53 % étaient de grade III et 82 % avaient un score HER2 3+ en immunohistochimie. Toutes les participantes, sauf un patient, étaient des femmes. Les patientes recevaient une chimiothérapie néoadjuvante toutes les trois semaines associant paclitaxel (J1 et J8), carboplatine (J1), trastuzumab et pertuzumab (J1), pour un maximum de neuf cycles. Une IRM mammaire était réalisée tous les trois cycles afin d’évaluer la réponse ; en cas de réponse radiologique complète, la chirurgie était effectuée précocement. Après la chirurgie, les patientes en réponse pathologique complète recevaient un traitement adjuvant par trastuzumab et pertuzumab pendant un an, tandis que celles présentant une maladie résiduelle poursuivaient la chimiothérapie jusqu’à neuf cycles au total, suivis de 14 cycles de trastuzumab emtansine.
Efficacité maintenue & toxicité réduite grâce à la désescalade
Après un suivi médian de 40,1 mois, 40 événements (9 %) ont été observés (19 chez les patientes RH− et 21 chez les RH+). La survie sans événement à 3 ans était de 92,2 % (IC 95 % : 88,7–95,9) chez les patientes RH− et de 92,0 % (88,5–95,6) chez les patientes RH+. Les taux étaient particulièrement élevés chez les patientes ayant reçu un à trois cycles : 96,1 % si RH− et 98,6 % si RH+, contre 89,2 % et 94,2 % respectivement après quatre à six cycles, et 90,6 % et 85,4 % respectivement après sept à neuf cycles. L’obtention d’une réponse pathologique complète était associée à une meilleure survie sans événement à 3 ans (94,8 % vs 87,5 % ; p = 0,0040). Sur le plan de la tolérance, 63 % des patientes ont présenté un événement indésirable de grade ≥ 3 (10 % de grade 4), principalement neutropénie (40 %), anémie (18 %) et diarrhée (13 %), avec une fréquence augmentant avec le nombre de cycles de chimiothérapie. La dégradation de la qualité de vie était également associée au nombre de cycles de chimiothérapie administrés.
Une stratégie prometteuse, particulièrement chez les RH-
L’étude TRAIN-3 montre ainsi que l’optimisation de la durée de la chimiothérapie néoadjuvante guidée par IRM est associée à une survie sans événement favorable à 3 ans chez les patientes atteintes d’un cancer du sein HER2 positif de stade II-III. Chez les patientes présentant une réponse radiologique complète précoce, la limitation du traitement à trois cycles semble possible sans compromettre l’efficacité, tout en réduisant significativement la toxicité et en préservant la qualité de vie. Cette approche apparaît particulièrement pertinente pour les tumeurs RH−, où la corrélation entre réponse radiologique et pathologique est forte. En revanche, pour les tumeurs RH+, des outils de suivi plus performants et un recul prolongé demeurent nécessaires afin d’optimiser la sélection des patientes et de confirmer le bénéfice à long terme, notamment concernant les récidives tardives. Ces résultats soutiennent une stratégie de désescalade thérapeutique chez des patientes soigneusement sélectionnées, permettant de réduire la charge de traitement tout en maintenant l’efficacité clinique.


-1761040885.jpg)