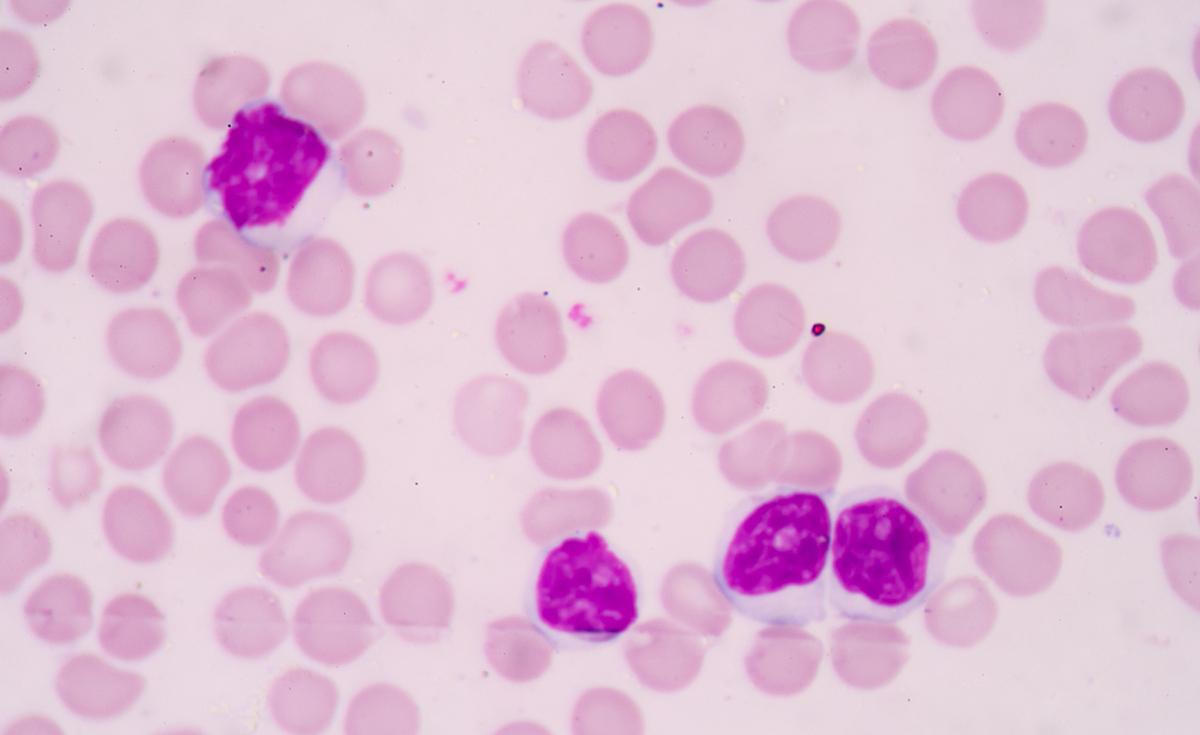
Hématologie
LLC/lymphome lymphocytique : combinaison GIVe en 1ère ligne chez des patients de haut-risque
L’essai CLL2-GIVe a évalué l’association à durée fixe d’une immunothérapie par Obinutuzumab, à une thérapie ciblée inhibant BCL2 (le Venetoclax) et un inhibiteur de BTK (Ibrutinib) lors du traitement de première ligne de patients atteints de leucémie lymphoïde chronique (LLC) ou de lymphome lymphocytique (LL) avec anomalie de TP53 (délétion 17p ou mutation TP53). Cet article décrit les principaux résultats cliniques (taux de réponse, taux de maladie résiduelle indétectable, données de survie sans-progression) de cet essai multicentrique.
- jitendrajadhav/istock
Les traitements par inhibiteurs de BTK (iBTK) et de BCL2 (iBCL2) ont remplacé les stratégies d’immunochimiothérapie dans le traitement des patients atteints de LLC/LL1,2. Ainsi, le Venetoclax, mimétique des BH3 inhibant la signalisation BCL2 et entraînant la mort cellulaire des cellules de LLC, a permis par combinaison aux anticorps monoclonaux anti-CD20 d’obtenir des maladies résiduelles (MRD) indétectables et des bénéfices significatifs de survie sans-progression chez les patients âgés et/ou comorbides et/ou en situation de rechute 2,3. D’autre part, son association avec les iBTK a également permis l’obtention de MRD indétectables et de durées prometteuses de réponse dans ce contexte 4,5.
Face à la nécessité d’essais cliniques prospectifs et randomisés évaluant l’efficacité et la tolérance des combinaisons en première ligne chez les patients dits de haut-risque (délétion 17p ou mutation TP53), les auteurs de l’étude CLL2-GIVe ont évalué l’association Obinutuzumab, Ibrutinib et Venetoclax (GIVe) chez des patients atteints de LLC et naïfs de traitement 6.
Une cohorte de haut-risque
Entre Septembre 2016 et Août 2018, 41 patients ont été inclus dans cette étude. Les patients recevaient 6 cycles d'induction par une combinaison triple GIVe, 6 cycles de consolidation par une association Ibrutinib et Venetoclax, puis 3 cycles d'Ibrutinib en monothérapie d’entretien jusqu'au restaging final (au cycle 15). Le maintien de l'Ibrutinib jusqu'au cycle 36 était conditionné à l'absence de réponse complète (RC) avec maladie résiduelle (MRD) indétectable au cycle 15. La durée médiane d'observation était de 38,4 mois (3,7-44,9 mois). L'âge médian au début de l'étude était de 62 ans (35-85) et 24 patients (58,5%) étaient des hommes.
Tous les patients étaient de haut-risque : 24 (58,5 %) avaient une del(17p) et une mutation TP53, 15 (36,6%) avaient une mutation TP53 isolée, et 2 patients (4,9%) avaient une del(17p) seule. Trente-deux patients (78,0%) présentaient un statut de la région variable du gène de la chaîne lourde de l'immunoglobuline (IGHV) non-muté. Les principaux critères d'évaluation étaient les taux de RC au cycle 15, les taux de réponse globale (RG), de MRD indétectable dans le sang et la moelle, puis les données de survie.
Des taux impressionnants de MRD indétectable et de survie sans-progression
Le taux de RC lors du restaging (au cycle 15) était 58,5% (95%CI, 42,1-73,7 ; P<0,001) et les taux de réponse partielle (RP) de 41,5% permettant d’obtenir un taux de RG objective de 100%.
Aux cycles 9 et 12, les taux de MRD indétectables sur le sang étaient respectivement de 87,8% et 78% tandis qu’au cycle 36, 43,9% des patients étaient en MRD indétectable et 29,3% des patients en MRD détectable dans le sang (26,8% des patients avaient des données manquantes en raison du décès, d’un nouveau traitement, de visites manquées en raison de la pandémie COVID19 ou encore d’une perte de suivi).
Avec un suivi médian de 38,4 mois (3,7-44,9), les taux de survie sans-progression (SSP) et de RG étaient respectivement de 79,9% et de 92,6%. Seulement 6 patients ont continué à prendre de l'ibrutinib au-delà du cycle 15.
Un profil de tolérance dominé par les cytopénies et les infections
Les effets indésirables (EI), tous grades confondus, ainsi que les EI de grade ≥3 les plus fréquents apparaissaient pendant la trithérapie d'induction et régressaient pendant la consolidation, puis l'entretien. Les EI de grade ≥3 les plus fréquents pendant toute la période de traitement étaient des neutropénies (48,8%), des thrombopénies (17,1%) et des infections (19,5%, notamment urinaires et respiratoires).
Les EI hématologiques de grade ≥3 les plus fréquents étaient la neutropénie (cycles 1-6, 41,5% ; cycles 7-12, 17,1% ; et cycle >13, 2,4%) et la thrombopénie (cycles 1-6, 17,1% et cycle >7, 0) ; tandis que les EI non hématologiques de grade ≥3 entre les cycles 1 et 6 étaient des syndromes de lyse tumorale biologique (9,8 %) et des réactions liées à la perfusion (7,3 %). La toxicité cardiovasculaire de grade ≥3 se manifestait notamment sous la forme de fibrillation auriculaire (2,4%) et d’hypertension artérielle (4,9%).
Conclusion
Les résultats de cette étude démontrent que l’association GiVe est une stratégie thérapeutique à durée fixe hautement efficace pour les patients atteints de LLC de haut risque (délétion 17p et/ou mutation TP53), avec un profil de tolérance attendu et acceptable.
Le nombre d'études portant spécifiquement sur les patients de haut-risque étant faible, d’autres essais seront nécessaires pour mieux définir une stratégie thérapeutique optimale dans ce contexte.
Références
- Burger JA, Barr PM, Robak T, et al. Long-term efficacy and safety of first-line ibrutinib treatment for patients with CLL/SLL: 5 years of follow-up from the phase 3 RESONATE-2 study. Leukemia 2020;34:787-98.
- Seymour JF, Kipps TJ, Eichhorst BF, et al. Enduring undetectable MRD and updated outcomes in relapsed/refractory CLL after fixed-duration venetoclax-rituximab. Blood 2022;140:839-50.
- Fischer K, Al-Sawaf O, Bahlo J, et al. Venetoclax and Obinutuzumab in Patients with CLL and Coexisting Conditions. N Engl J Med 2019;380:2225-36.
- Kater AP, Levin MD, Dubois J, et al. Minimal residual disease-guided stop and start of venetoclax plus ibrutinib for patients with relapsed or refractory chronic lymphocytic leukaemia (HOVON141/VISION): primary analysis of an open-label, randomised, phase 2 trial. Lancet Oncol 2022;23:818-28.
- Rogers KA, Huang Y, Ruppert AS, et al. Phase II Study of Combination Obinutuzumab, Ibrutinib, and Venetoclax in Treatment-Naive and Relapsed or Refractory Chronic Lymphocytic Leukemia. J Clin Oncol 2020;38:3626-37.
- Huber H, Tausch E, Schneider C, et al. Final analysis of the CLL2-GIVe trial: obinutuzumab, ibrutinib, and venetoclax for untreated CLL with del(17p)/TP53mut. Blood 2023;142:961-72.