Onco-dermatologie
Carcinome épidermoïde cutané métastatique : actualités dans l’immunothérapie à l’ASCO 2020
Le congrès de l’ASCO 2020 qui s’est tenu en juin dernier a permis de faire le point sur les avancées en immunothérapie pour le traitement du carcinome épidermoïde cutané métastatique
- Istock/libre de droit
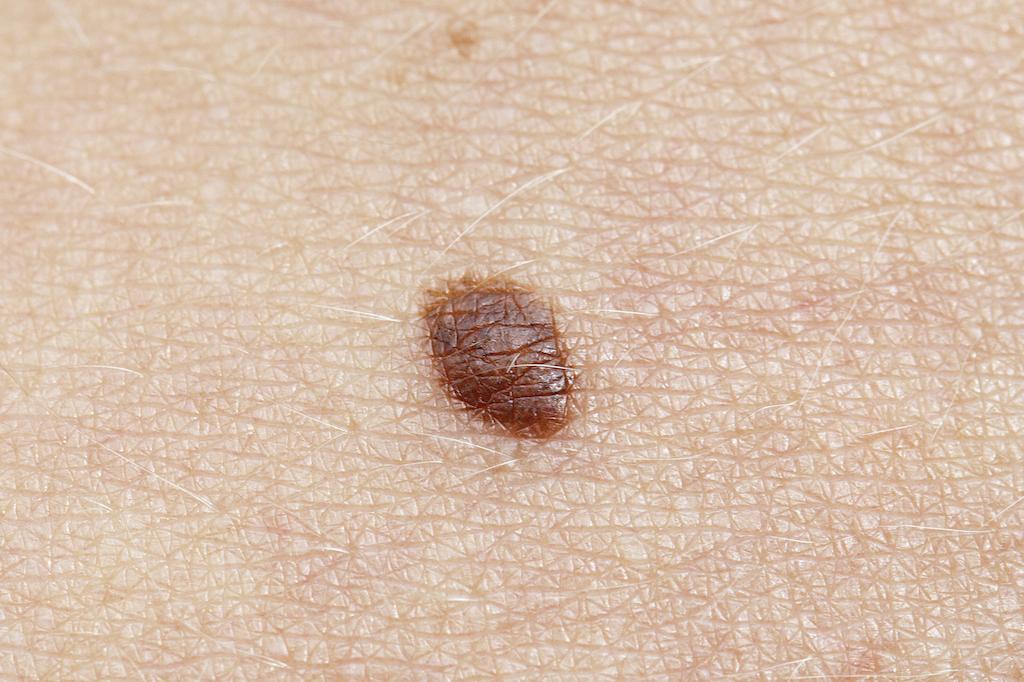
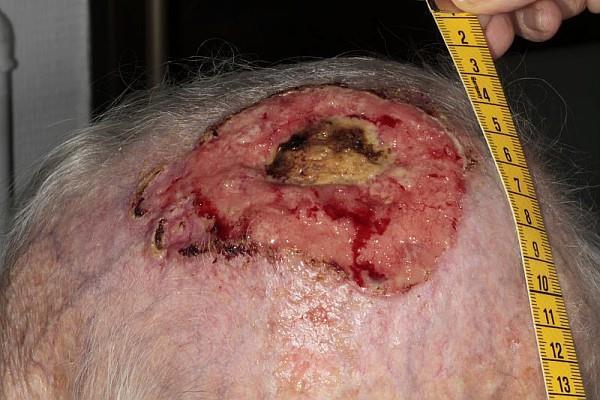
Le traitement du carcinome épidermoïde cutané (CEC) avancé inopérable ou métastatique a changé ces dernières années avec l’arrivée d’une immunothérapie anti-PD1, le cemiplimab, approuvé en Europe et en France.
Des données qui confirment l’intérêt du cemiplimab
L’actualisation à 3 ans des données de l’étude de phase 2 ayant permis d’obtenir la mise sur le marché du cemiplimab a été présentée au dernier congrès de l’ASCO. Elle portait sur les 3 premiers groupes de patients : cemiplimab 3mg/kg toutes les 2 semaines pendant 96 semaines pour les CEC métastatiques (CECm) (groupe 1) et CEC localement avancés (groupe 2) et cemiplimab 350 mg toutes les 3 semaines pendant 54 semaines pour les CECm (groupe 3). La médiane de suivi était de 51.7 mois, 193 patients étaient inclus. Le taux de réponse objective pour l’ensemble des patients était de 46.1 % (intervalle de confiance 95% (IC95) = 38.9-53.4), dont 16.1% de réponse complète (RC). La survie sans progression (SSP) était de 18.4 mois (IC95 = 10.3-24.3) et la médiane de survie globale (SG) n’était pas atteinte. La probabilité de SG à 24 mois était de 73.3%. Le profil de tolérance était rassurant avec des résultats similaires aux autres anti-PD1, 48.7% ont eu un effet indésirable de grade 3 ou plus.
Une analyse post-hoc de cette étude, s’intéressant à la qualité de vie des malades a démontré la réduction significative de la douleur et l’amélioration de la qualité de vie dès le 3e cycle de perfusion, se maintenant au cours du traitement.
Un autre anti PD1 bientôt disponible ?
L’essai CA209-9JC, évaluant l’intérêt du nivolumab, un autre anti-PD1, à la dose de 3 mg/kg toutes les 2 semaines, pendant 12 semaines, a montré des résultats du même ordre dans la même indication. Sur les 22 patients évaluables, 54.5% avaient obtenu une réponse partielle, mais aucune RC. Le taux de contrôle de la maladie, incluant les malades stables, était de 77%. Les médianes de SSP et SG n’étaient pas atteintes, et le profil de toxicité était semblable aux études antérieures, avec un taux d’effets indésirables de grade 3 ou plus de 21%, inférieur à l’étude évaluant le cemiplimab ci-dessus.
Plus loin dans le futur …
Enfin, l’essai C-POST, actuellement ouvert aux inclusions, a été présenté. Il s’agit d’un essai de phase 3, randomisé contre placebo, évaluant l’intérêt du cemiplimab 350mg toutes les 3 semaines en adjuvant pour les CEC à haut risque de récidive ou de métastase, après chirurgie et radiothérapie. L’objectif principal est la survie sans maladie. Une autre étude, KEYNOTE-630, évalue l’intérêt du pembrolizumab, un autre anti-PD1, en adjuvant dans la même indication.
L’intérêt de l’immunothérapie dans le traitement du CEC avancé ou métastatique se renforce avec l’actualisation des données de survie à 3 ans et le développement d’autres anti-PD1 dans cette indication. Près de la moitié des patients obtiennent une réponse au traitement. Les premières données en adjuvant, après chirurgie et radiothérapie, devraient être connues dans les prochaines années.