Onco-Digestif
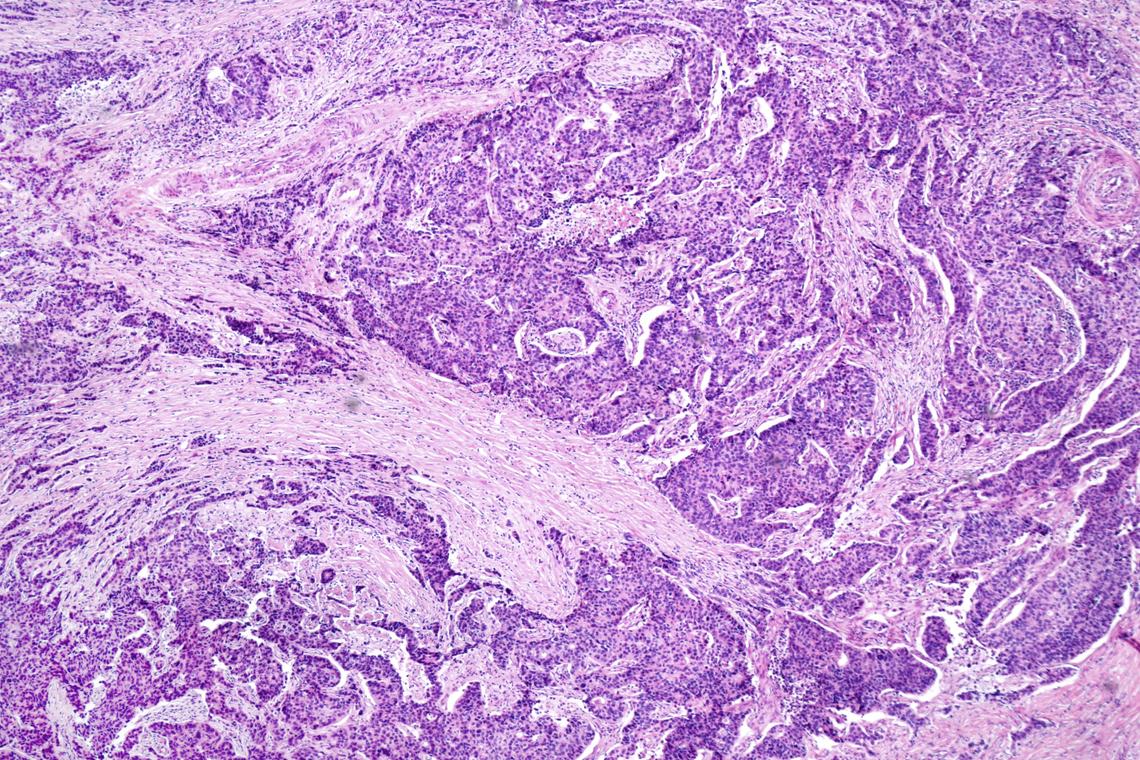
Adénocarcinome péri-ampullaire réséqué : chimiothérapie adjuvante + / - chimiothérapie
La question du traitement adjuvant optimal des adénocarcinomes pancréatiques divise Europe et Etats-Unis depuis des années. En effet, la chimioradiothérapie (CRT) continue à être utilisée aux Etats-Unis alors qu’elle a été supplantée par la chimiothérapie en Europe depuis les résultats des essais ESPAC-1, CONKO-001 puis PRODIGE 24 (1-3). Cette année à l'ASCO, Karyn Goodman a présenté les résultats de l’essai NRG-RTOG 0848 qui étaient attendus depuis longtemps [Abrams RA et al. Abstract 4005].

- mi-viri/iStock
En 2008, les Américains ont conçu l’essai RTOG 0848 afin d’évaluer le bénéfice d’une CRT après 6 mois de chimiothérapie adjuvante par gemcitabine qui était le standard à cette époque. Dans cet essai de phase III étaient inclus des patients ayant eu une résection macroscopiquement complète d’un adénocarcinome de la tête du pancréas (résection R0 ou R1), en bon état général (OMS 0-1) et avec un taux de CA19-9 post-opératoire < 180. Ils étaient randomisés une première fois entre 5 cycles de gemcitabine et 5 cycles de gemcitabine + erlotinib.
En 2014, suite aux résultats de l’essai LAP07 ayant montré l’absence de bénéfice de l’erlotinib pour les cancers localement avancés, cette première randomisation a été supprimée. Après la 2ème randomisation, en l’absence de progression tumorale, les patients recevaient soit un cycle supplémentaire de gemcitabine, soit un cycle de gemcitabine suivie d’une CRT à la dose de 50,4 Gy avec de la capécitabine en concomitant. Ils étaient stratifiés en fonction du statut ganglionnaire, du taux de CA19-9, du statut des marges et du type de chimiothérapie adjuvante. Il y avait un contrôle de qualité en temps réel de la radiothérapie.
L’objectif principal était le taux de survie globale. L’hypothèse statistique était de montrer un allongement de la médiane de survie globale de 17,5 à 22,5 mois dans le bras CRT. Les objectifs secondaires étaient la survie sans maladie et la toxicité aiguë.
Une amélioration de la survie globale chez les patients N0
Entre 2009 et 2018, 546 patients ont été inclus dans cette étude. Les caractéristiques des patients étaient comparables entre les deux bras. Il faut souligner que le taux de résection R1 était de 17 % seulement, faisant suspecter une sous-estimation du taux de marges envahies. Le suivi médian était de 2,2 ans. Le taux de survie globale à 5 ans n’était pas amélioré dans le bras CRT (cf. tableau).
|
|
Chimiothérapie n = 174 |
Chimiothérapie + CRT n = 180 |
p |
|
Taux de survie globale à 5 ans |
23 % |
28 % |
0,38 |
|
Taux de survie sans maladie à 5 ans |
15 % |
21 % |
0,045 |
|
Taux de survie globale à 5 ans pour les patients pN0 |
29 % |
48 % |
0,03 |
|
Taux de survie sans maladie à 5 ans pour les patients pN0 |
19 % |
47 % |
0,004 |
Par contre, le taux de survie sans maladie à 5 ans était significativement meilleur dans le bras CRT. Il existait un bénéfice de la CRT en termes de survie pour les patients pN0 mais pas pour les pN1. Le taux de toxicité aiguë de grade > 3 était significativement plus élevé dans le bras CRT (43 % versus 24 %, p < 0,001). La CRT adjuvante pourrait donc avoir un intérêt après chimiothérapie adjuvante chez les patients N0, ayant à priori une maladie localisée. Ces résultats sont à vérifier avec une chimiothérapie plus efficace telle que le FOLFIRINOX.
Références
- Neoptolemos JP, Dunn JA, Stocken DD, Almond J, Link K, Beger H, et al. Adjuvant chemoradiotherapy and chemotherapy in resectable pancreatic cancer: a randomised controlled trial. Lancet 2001;358(9293):1576-85.
- Oettle H, Post S, Neuhaus P, Gellert K, Langrehr J, Ridwelski K, et al. Adjuvant chemotherapy with gemcitabine vs observation in patients undergoing curative-intent resection of pancreatic cancer: a randomized controlled trial. JAMA 2007;297(3):267-77.
- Conroy T, Hammel P, Hebbar M, Ben Abdelghani M, Wei AC, Raoul JL, et al. FOLFIRINOX or Gemcitabine as Adjuvant Therapy for Pancreatic Cancer. N Engl J Med 2018;379(25):2395-406.