Hématologie
Myélome multiple réfractaire : un CAR-T cells plus efficace que les traitements de rattrapage standard
La thérapie par cellules T à récepteur antigénique chimérique (Chimeric Antigen Receptor T-cells, ou CAR-T cells) est un traitement novateur, de développement récent pour la prise en charge du myélome multiple en rechute ou réfractaire (MMRR). Cet essai randomisé, appelé KarMMa-3, confirme la supériorité de cette approche en comparaison aux traitements de rattrapage standard.
- Meletios Verras/istock
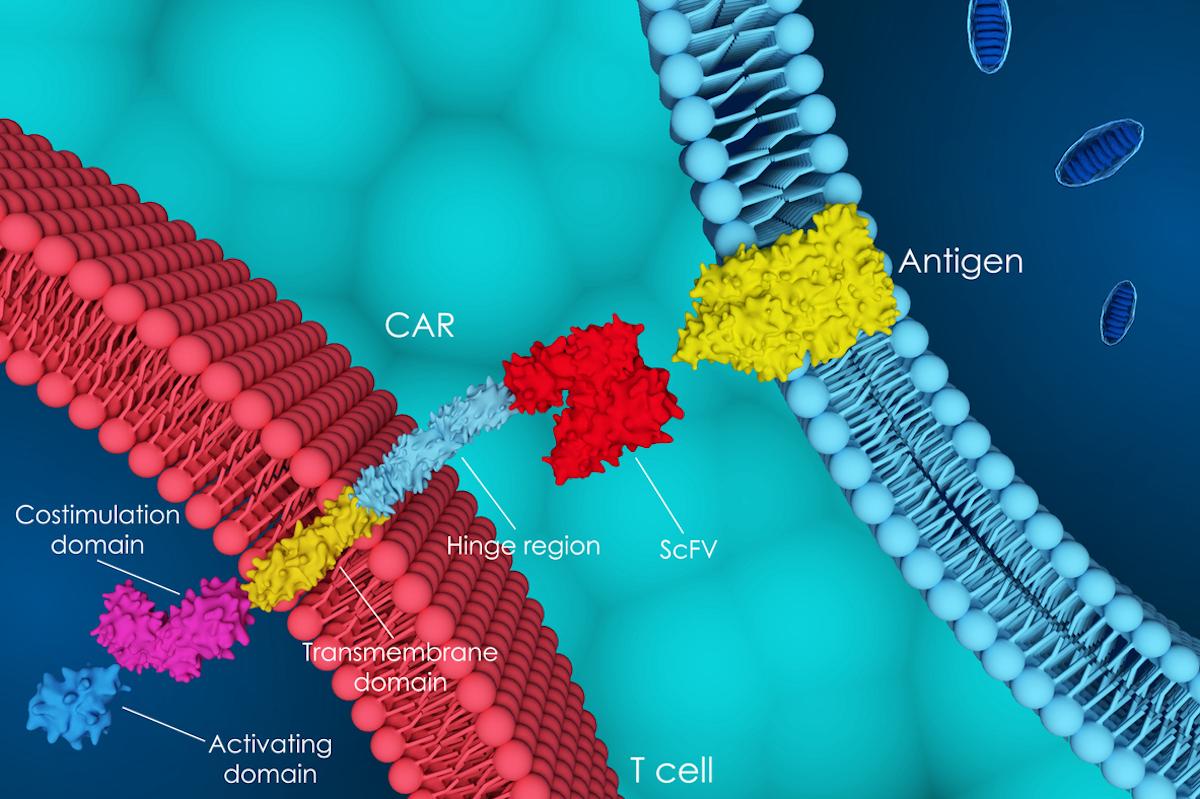
L’idecabtagene-vicleucel (ide-cel ; bb2121) est un CAR-T cell autologue qui possède un domaine extra-cellulaire de reconnaissance du BCMA, un domaine de costimulation de type 4-1BB et un domaine de signalisation intracytoplasmique CD3V. L’ide-cel est disponible depuis 2021 pour la prise en charge des patients atteints de MMRR ayant reçu au moins 3 traitements antérieurs dont un immunomodulateur (IMiD), un inhibiteur du protéasome (IP), et un anticorps monoclonal anti-CD38, dits « triple-exposés ».
Les données issues des essais cliniques et d’un essai en vie réelle ont montré que l’ide-cel permettait d’obtenir des réponses profondes et prolongées dans cette population, dont la durée médiane de survie est inférieure à 1 an (Munshi et al, NEJM 2021 ; Hansen et al JCO 2023).
Des patients atteints de MM à un stade avancé
Dans l’essai KarMMa-3, 386 patients avec un MMRR ont été randomisés pour recevoir un traitement par ide-cel (n=254) ou un traitement de rattrapage standard (n=132), parmi 5 combinaisons triples au choix de l’investigateur comportant IP, anti-CD38, IMiDs et/ou elotuzumab. Au total, 225 patients ont effectivement reçu l’ide-cel à une dose médiane de 445×106 CAR- T cells (min-max, 175×106 - 529×106) et 126 ont reçu le traitement standard.
L’âge médian était de 63 ans. Il s’agissait d’une population atteinte de MMRR avancé : le délai médian depuis le diagnostic était de 4 ans ; 24% des patients avaient une maladie extra-médullaire ; 42% des patients du groupe ide-cel et 46% des patients du groupe standard présentaient une cytogénétique de haut risque. Les patients avaient reçu en médiane 3 lignes de traitement antérieurs (min-max, 2-4) ; 65 et 67% avaient une maladie triple-réfractaire, et 6 et 4% penta-réfractaire, dans les groupes ide-cel et standard, respectivement.
L’ide-cel est plus efficace que le traitement standard
Après un suivi médian de 18,6 mois, la survie sans progression médiane est de 13,3 mois pour les patients traités par ide-cel et 4,4 mois pour les patients traités par un rattrapage standard. Le taux de réponse globale est de 71% des patients traités par ide-cel, dont 39% de réponse complète, contre 42% et 5%, respectivement, pour le traitement standard. Cet avantage est maintenu dans les différents sous-groupes (cytogénétique de haut risque, atteinte extra-médullaire…).
Un profil de toxicité attendu
La toxicité hématologique est plus importante dans le groupe ide-cel (neutropénie, 78 vs 44% ; anémie, 66 vs 36% ; thrombopénie, 54 vs 29%) ; le taux d’infection était similaire (58 vs 54%). Dans le groupe ide-cel, un syndrome de relargage cytokinique est rapporté chez 88% des patients, et une neurotoxicité chez 15%, similaire aux taux rapportés dans les autres études.
Ces résultats confirment l’efficacité des CAR-T cells en comparaison aux traitements standards dans cette population de patients avec un MMRR et triples-exposés.