Onco-dermatologie
Mélanome au stade avancé : quelles avancées en adjuvant ?
La prise en charge du mélanome au stade avancé a connu de grandes avancées ces dernières années grâce aux immunothérapies. Où en est on aujourd'hui du traitement adjuvant ?
- Istock/Christoph Burgstedt
La prise en charge thérapeutique du mélanome au stade avancé a connu ces dernières années une véritable révolution. Depuis 2010, le développement de deux types d’approches (thérapie ciblée et immunothérapie) a permis un allongement significatif de la survie globale des patients atteints de mélanome avancé.
Ces mêmes approches thérapeutiques (thérapie ciblée et immunothérapie) ont été proposées plus récemment en situation adjuvante à des malades identifiés à haut risque de récidive.
Quatre essais de traitement adjuvant
Quatre essais prospectifs randomisés en double aveugle incluant des patients atteints de mélanome ganglionnaire et/ou avancé complétement réséqué, donc à haut risque de récidive, et traités en situation adjuvante ont ainsi été publiés entre 2017 et 2019 :
1. essai EORTC : comparant l’ipilimumab (anti-CTLA4) 10mg/kg à un placebo (951 patients)2,
2. essai Combi-AD : comparant l’association dabrafenib et trametinib (thérapie ciblée combinée anti-BRAF et anti-MEK) à un placebo (870 patients)3,
3. essai Checkmate 238 : comparant le nivolumab (anti-PD1) 3mg/kg/2 semaines à l’ipilimumab 10mg/kg/3 semaines (traitement considéré « de référence » suite aux résultats de l’essai EORTC ci-dessus) (906 patients)4,
4. essai Keynote 054 : comparant le pembrolizumab (anti-PD1) 200mg/3 semaines à un placebo (1019 patients)5.
Dans l’essai EORTC, le traitement par ipilimumab était réalisé toutes les 3 semaines, 4 fois, puis selon un schéma d’entretien tous les 3 mois pendant 3 ans maximum. Dans les trois autres essais (Combi-AD, Checkmate 238 et Keynote 054), la durée de traitement était de 1 an.
Quels bénéfices pour quels patients ?
Les critères d’inclusion et notamment le stade de la maladie diffèrent en fonction des essais. Ainsi, les essais EORTC, Combi-AD et Keynote 054 incluaient des patients atteints de mélanome stade IIIA, IIIB ou IIIC (atteinte ganglionnaire y compris ganglion sentinelle envahi sur au moins 1mm) avec la restriction d’une mutation BRAF V600E/K pour l’essai Combi-AD. L’essai Checkmate 238 incluait également des patients ayant un mélanome ganglionnaire mais également métastatique (stade IV) complétement réséqué.
Les deux premiers essais montrent un allongement significatif de la survie globale et sans récidive des patients recevant le traitement. A 7 ans, 39,2% des patients n’ont pas récidivé dans le bras ipilimumab vs 30,9% dans le bras placebo (hazard ratio 0,75 ; p<0,001). A 4 ans, 54% des patients traités par dabrafenib-trametinib en adjuvant n’ont pas récidivé vs 38% des patients traités par placebo (hazard ratio 0,49). L’ipilimumab a eu par la suite l’autorisation aux Etats-Unis en adjuvant à la dose de 10mg/kg mais pas en Europe du fait d’une toxicité notable (54% de patients avec une toxicité grade III ou IV).
Le recul est moindre dans les 2 autres essais avec une efficacité significative uniquement sur la survie sans récidive pour les deux anti-PD1. Ainsi, à 2 ans, 62,6% des patients traités par nivolumab n’ont pas récidivé en comparaison aux 50,2% des patients traités par ipilimumab (hazard ratio 0,65 ; p < 0,001). Avec 18 mois de recul, 71,4% des patients traités par pembrolizumab n’ont pas récidivé en comparaison à 53,2% des patients traités par placebo (HR 0,57 ; p < 0,001).
Situation actuelle pour les patients
En France, les trois traitements (association dabrafenib-trametinib, nivolumab et pembrolizumab) ont désormais l’AMM et le remboursement dans l’indication « Mélanome de stade III avec atteinte ganglionnaire ayant eu une résection complète ». Le nivolumab a en plus l’indication pour les patients atteints de mélanome métastatique (stade IV) après résection complète.
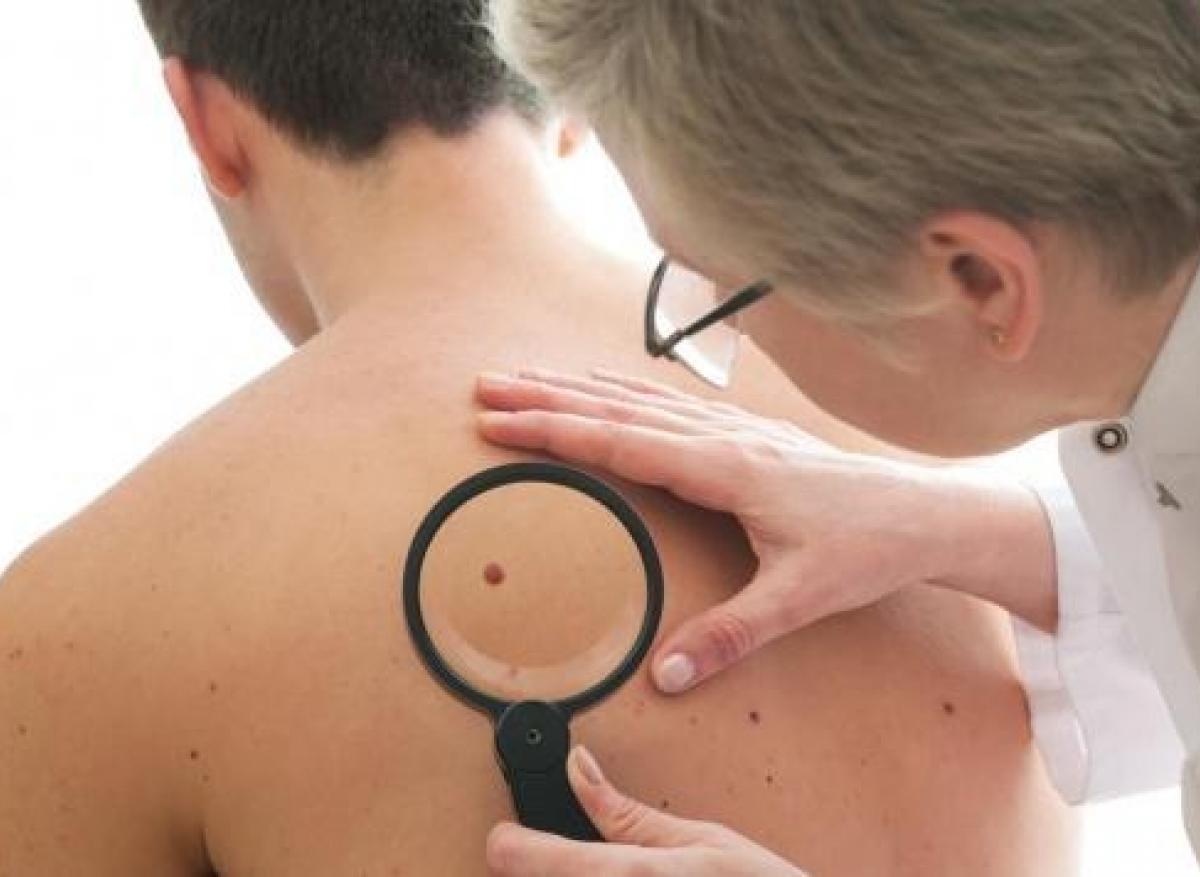
Ces résultats ont conduit à une modification des pratiques et notamment à la généralisation de la pratique du ganglion sentinelle dans la prise en charge initiale du mélanome avec désormais un impact thérapeutique. En effet, la technique de ganglion sentinelle était pratiquée antérieurement dans de nombreux centres avec un objectif de stadification de la maladie. Depuis ces progrès, l’envahissement du ganglion sentinelle par du mélanome (sur au moins 1mm) correspond désormais à une indication de traitement adjuvant pendant 1 an.
En pratique, la technique du ganglion sentinelle est recommandée de façon formelle dans le même temps opératoire que la reprise cutanée pour les mélanomes ulcérés quel que soit l’indice de Breslow ou avec un Breslow supérieur ou égal à 1mm. L’indication est à discuter en cas de Breslow entre 0,8 et 1mm6.
Questions restant en suspens
Ces résultats sont très encourageants et permettent (enfin !) de pouvoir proposer aux patients atteints de mélanome à haut risque un traitement adjuvant. Cependant, ces nouvelles approches sont aussi à l’origine de beaucoup de questions restant en suspens pour l’instant.
Ainsi, quel est le « meilleur » traitement adjuvant chez un patient BRAF muté ? On peut en effet en théorie proposer soit la thérapie ciblée soit l’immunothérapie. En l’absence d’étude comparative des deux approches, le choix fait aujourd’hui appel à d’autres critères (coût, compliance et choix du patient…).
On peut également se poser la question de l’intérêt de ces traitements à des stades encore plus précoces (mélanomes primitifs stade IIB et IIC avec ganglion sentinelle négatif). Deux essais sont actuellement en cours et comparent un traitement par anti-PD1 (respectivement pembrolizumab ou nivolumab) à un placebo chez ces patients (essais Keynote-716 NCT03553836 et Checkmate 209-76K NCT04099251).
Enfin, des petites séries récentes d’approches néoadjuvantes ont montré des résultats encourageants et le positionnement des stratégies néoadjuvantes et/ou adjuvantes chez un patient atteint de mélanome ganglionnaire macroscopique sera un des enjeux futurs