Onco-Digestif
Cancer du côlon métastatique BRAF muté : actualisation de l’essai BREAKWATER
Dans le cancer du côlon métastatique BRAFV600E, l’intérêt d’une association encorafenib + cétuximab + FOLFOX ou FOLFIRI est actuellement étudiée. Des résultats préliminaires montrent que cette association n’engendre pas de surtoxicité.
- Mohammed Haneefa Nizamudeen/iStock
Sur la base de l'étude phase 3 BEACON, l'inhibiteur BRAF encorafenib (E) associé à l’anti-EGFR cétuximab (C) a été approuvé en France comme traitement des patients pré-traités avec chimiothérapie atteints de cancer colorectal métastatique BRAFV600E muté.
Les résultats de l’étude de Safety Lead-in de l’essai de phase 3 BREAKWATER, ont été présentés à l’ESMO 2022. Cette étude évalue l'association encorafenib + cétuximab à la chimiothérapie FOLFOX/FOLFIRI opposée à une chimiothérapie standard dans le cancer du côlon métastatique BRAFV600E muté.
Une association encorafenib, cétuximab et chimiothérapie
Les patients ont reçu 300 mg d’encorafenib par jour + 500 mg/m2 de cétuximab toutes les 2 semaines + mFOLFOX6 (EC + mFOLFOX6) ou FOLFIRI (EC + FOLFIRI), au choix de l’investigateur, toutes les 2 semaines, jusqu'à une progression de la maladie ou une toxicité inacceptable en première ou deuxième ligne.
Le critère d'évaluation principal était la fréquence des toxicités limitant la dose (DLT). Les critères d'évaluation secondaires comprenaient la sécurité, la pharmacocinétique et l'activité antitumorale.
Pas d'augmentation de la toxicité
Des effets indésirables graves (EIG) ont été recensés chez 48,1% (EC + mFOLFOX6) et 33,3% (EC + FOLFIRI) des patients, et des EIG liés au traitement (tous médicaments confondus) chez 25,9% (EC + mFOLFOX6) et 13,3% (EC + FOLFIRI) des patients. Une toxicité limitant la dose (neutropénie de grade ≥3) a été observé dans le bras EC + FOLFIRI.
Par ailleurs, l’étude pharmacocinétique a mis en évidence une diminution de la concentration du SN38 en raison d’une interaction connue avec l’encorafénib liée au CYP3A. Les données sur l'activité antitumorale figurent dans le tableau ci-dessous.
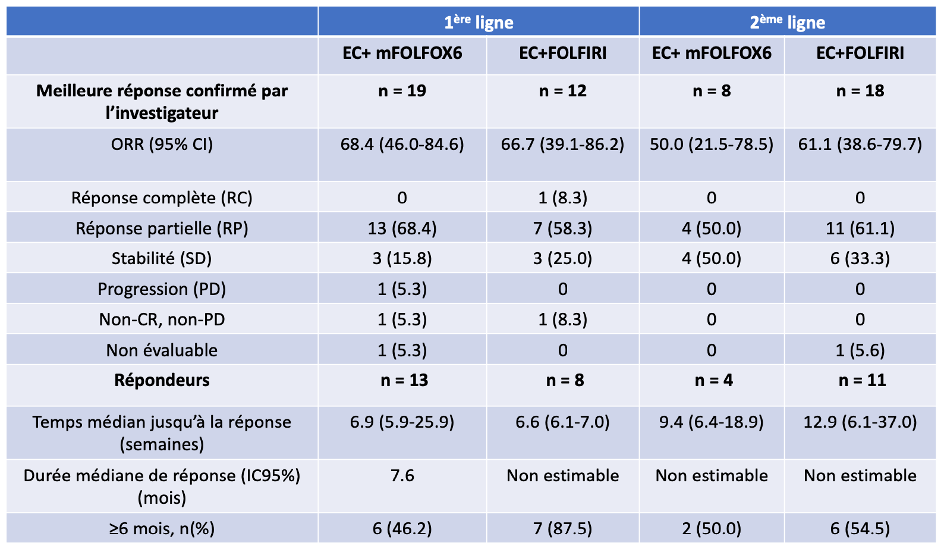
Tableau 1 : Activité anti-tumorale de l’association EC+ chimiothérapie (d’après LBA26, Annals of Oncology (2022) 33 (suppl_7): S808-S869. 10.1016/annonc/annonc1089.
Des résultats prometteurs à confirmer
En conclusion, il n’y a pas eu de surtoxicité constatée avec l'association EC + chimiothérapie. Cette tolérance acceptable, couplée à une activité antitumorale préliminaire prometteuse, est en faveur de la poursuite de l’essai de phase 3 BREAKWATER (NCT04607421) en première ligne métastatique des cancers du côlon BRAFV600E mutés, ouvert aux inclusions à l’international (mais pas en France…).