Dermatologie
Hidradénite suppurée : l'efficacité du povorcitinib se consolide jusqu'à 54 semaines
L'arrivée potentielle d'un inhibiteur JAK1 oral dans l'HS représenterait en clinique un changement de paradigme thérapeutique : une alternative aux injections, avec une administration orale quotidienne, un profil d'efficacité progressif et soutenu, et une tolérance acceptable dans la durée.
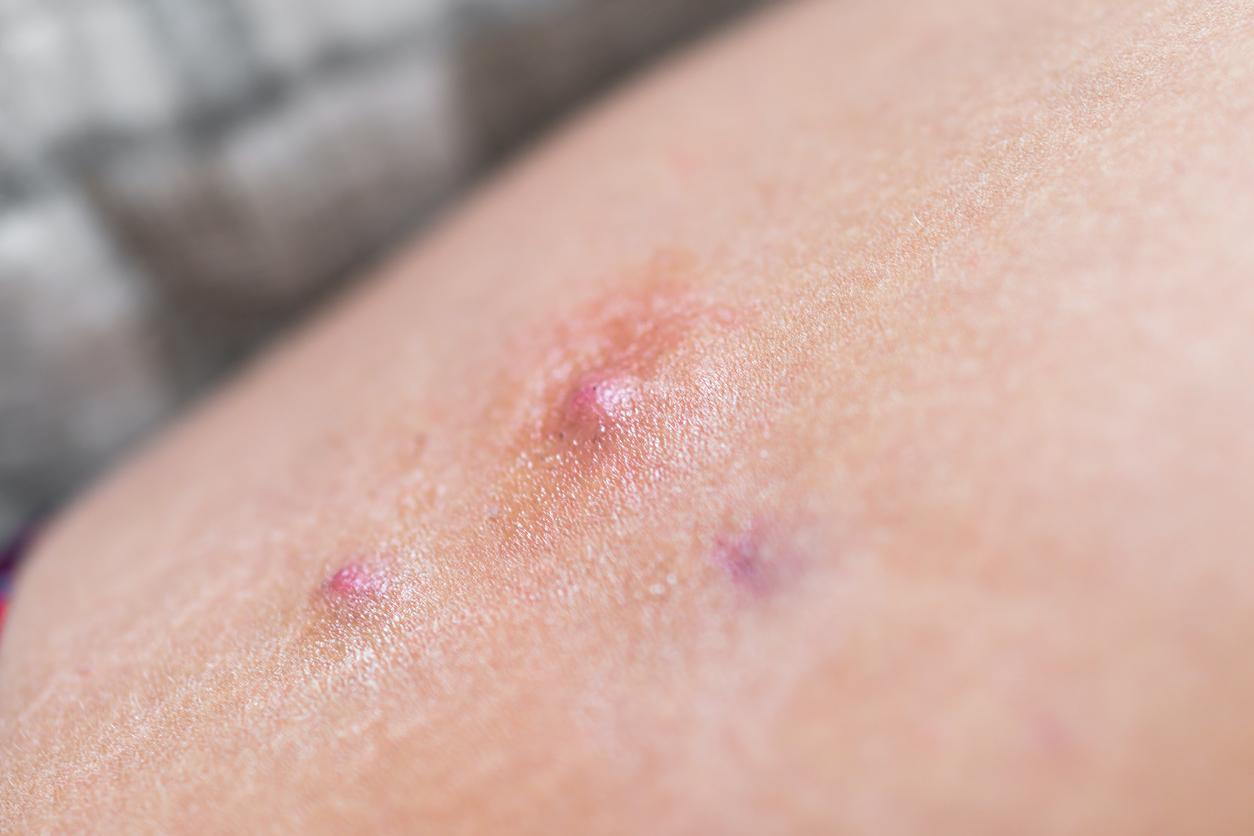
- krblokhin/iStock
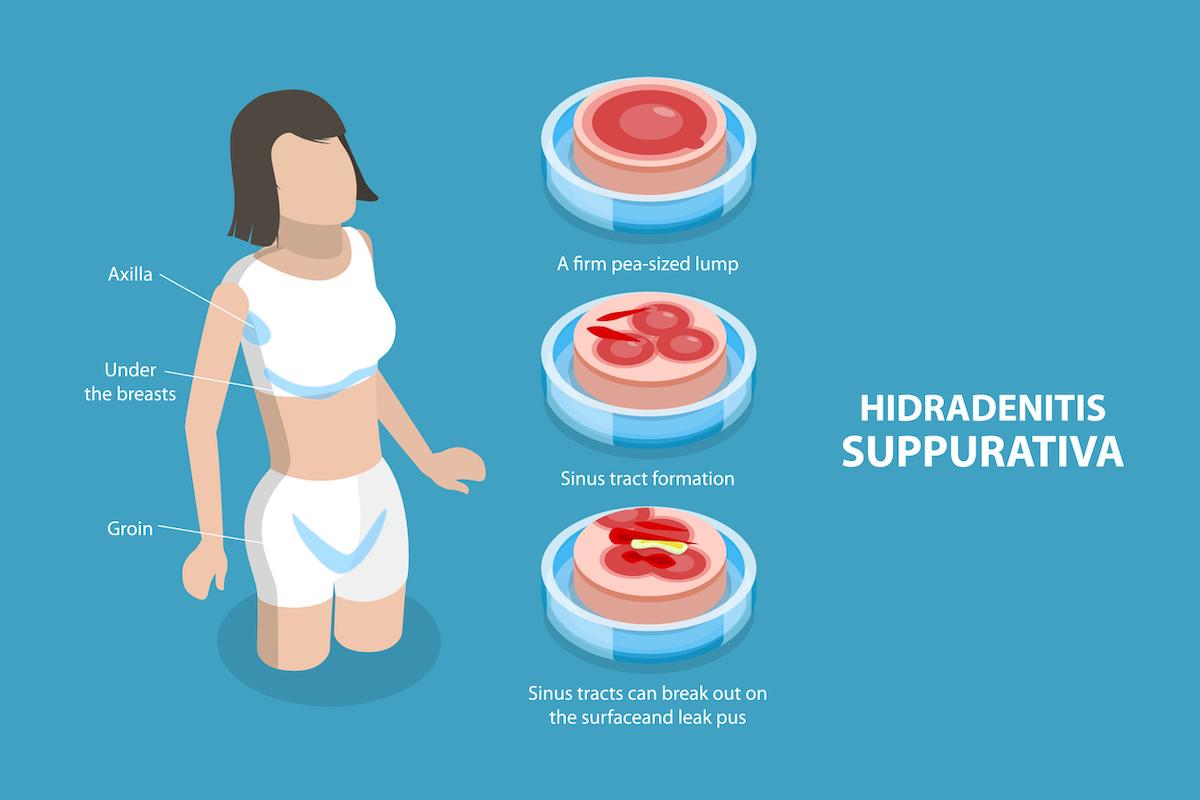
L'hidradénite suppurée (HS) modérée à sévère reste l'une des dermatoses inflammatoires chroniques les plus invalidantes, caractérisée par des nodules douloureux, des abcès récidivants et des fistules dont l'impact sur la qualité de vie est important. Si les biothérapies anti-TNF et anti-IL-17 ont représenté une avancée majeure, l'absence de traitement oral efficace constitue toujours une lacune thérapeutique importante. C'est dans ce contexte que les données à 54 semaines du povorcitinib, présentées en session de dernière minute au congrès annuel 2026 de l'American Academy of Dermatology (AAD) à Denver, suscitent un intérêt particulier.
Le povorcitinib (laboratoire Incyte) est un inhibiteur oral hautement sélectif de JAK1, administré une fois par jour. Son développement repose sur la place centrale de la voie JAK-STAT dans la physiopathologie de l'HS, notamment via les cytokines IL-6, IL-17 et IFN-γ qui activent préférentiellement JAK1. La sélectivité pour JAK1 est recherchée pour optimiser le rapport bénéfice-risque en réduisant les effets de classe liés à l'inhibition des autres isoformes JAK. La molécule est par ailleurs en développement clinique dans d'autres indications dermatologiques, dont le vitiligo et le prurigo nodulaire, ainsi que dans l'asthme modéré à sévère.
Les deux études pivots de phase 3, STOP-HS1 et STOP-HS2, ont chacune inclus environ 600 adultes présentant une HS modérée à sévère diagnostiquée depuis au moins trois mois, avec un nombre total d'adénomes et de nodules inflammatoires (AN) supérieur ou égal à 5, des lésions présentes dans au moins deux zones anatomiques distinctes et une réponse insuffisante aux traitements systémiques antérieurs. La population était représentative des patients rencontrés en pratique courante : âge moyen de 37 ans, majorité féminine, près de trois quarts de patients de peau blanche, durée moyenne de la maladie de dix ans. Aucun antibiotique n'a été autorisé pendant l'essai en dehors du traitement de secours.
Les patients ont été randomisés selon un ratio 1:1:1 pour recevoir soit 45 mg, soit 75 mg de povorcitinib par jour, soit un placebo, pendant une première phase de 12 semaines en double aveugle. Une période d'extension de 42 semaines a ensuite suivi, portant la durée totale de suivi à 54 semaines. Les patients initialement sous placebo ont été réaffectés à l'une ou l'autre des doses actives au terme de la phase aveugle, tandis que ceux sous traitement actif ont poursuivi leur dose initiale.
Le critère d'évaluation principal des deux études — la réponse HiSCR50 à 12 semaines, définie par une réduction d'au moins 50 % du nombre total d'abcès et de nodules inflammatoires sans augmentation des abcès — avait été atteint avec une supériorité statistiquement significative des deux doses de povorcitinib sur le placebo. Ces résultats avaient d'ores et déjà établi la preuve d'efficacité à court terme et positionné la molécule parmi les candidats sérieux à l'obtention d'une AMM dans cette indication.
Une réponse qui s'approfondit dans le temps
Ce qui distingue les nouvelles données présentées à Denver par le Dr Martina J. Porter (Beth Israel Deaconess Medical Center, Boston) tient à la trajectoire évolutive de la réponse. Contrairement à ce qui est parfois observé avec d'autres traitements où les taux de réponse plafonnent ou s'érodent après la phase initiale, le povorcitinib a démontré une amélioration continue jusqu'à la semaine 54. Jusqu'à 71,4 % des participants ont atteint le seuil HiSCR50 à cette échéance, témoignant d'un effet thérapeutique qui se consolide avec la durée d'exposition. Plus remarquable encore, les seuils de réponse plus exigeants ont également progressé : jusqu'à 57 % des patients ont atteint HiSCR75 et jusqu'à 29 % HiSCR100 — ce dernier seuil correspondant à une quasi-disparition de la charge inflammatoire.
Un résultat particulièrement significatif sur le plan clinique concerne la disparition complète des lésions inflammatoires (score ANdT = 0, c'est-à-dire absence de tout nodule inflammatoire, abcès ou fistule) : ce critère a été atteint par 16 % à 20 % des patients à la semaine 54. Pour une pathologie réputée aussi réfractaire aux traitements systémiques, ce niveau de réponse complète est remarquable. La résolution des trois composantes lésionnelles — nodules, abcès et fistules — a été observée de façon constante. Des améliorations cliniquement significatives ont également été documentées sur les symptômes associés : douleurs cutanées, fatigue et qualité de vie globale.
Moins de 10 % des patients ont arrêté le traitement
La sécurité à long terme constitue un point de vigilance majeur pour tout inhibiteur de JAK, au regard des signaux de classe identifiés dans d'autres indications (risque cardiovasculaire, thrombo-embolique, infectieux et carcinologique). Les données à 54 semaines sont ici rassurantes : les événements indésirables survenus pendant la période d'extension étaient globalement similaires, en nature et en intensité, à ceux rapportés à la semaine 12. Les effets indésirables les plus fréquents étaient l'acné, les rhinopharyngites et les infections des voies respiratoires supérieures, généralement d'intensité légère à modérée. Le taux d'événements indésirables graves sous traitement oscillait entre 3,7 % et 6,4 %, et moins de 10 % des patients ont arrêté le traitement. Les événements cardiovasculaires majeurs (MACE), les événements thrombo-emboliques et les événements malins, dont le zona, sont restés peu fréquents sans qu'aucun nouveau signal de sécurité n'ait été identifié. Ce profil est cohérent avec la sélectivité JAK1 du povorcitinib.
Ces données robustes à 54 semaines renforcent considérablement le dossier clinique du povorcitinib et nourrissent les attentes d'une soumission réglementaire prochaine. Le Dr Jennifer Hsiao (Keck School of Medicine, USC), investigatrice de STOP-HS2, souligne l'importance clinique des seuils de réponse élevés observés, rappelant qu'une amélioration partielle peut être insuffisante pour restaurer une qualité de vie satisfaisante. Elle appelle à des données de suivi à deux ans et au-delà, ainsi qu'aux résultats de l'étude de phase 2 en cours chez les adolescents — population particulièrement vulnérable et pour laquelle l'arsenal thérapeutique oral reste très limité.
L'arrivée potentielle d'un inhibiteur JAK1 oral dans l'HS représenterait en clinique un changement de paradigme thérapeutique : une alternative aux injections, avec une administration orale quotidienne, un profil d'efficacité progressif et soutenu, et une tolérance acceptable dans la durée. Les dossiers d'AMM et de remboursement détermineront la place réelle de cette molécule dans les algorithmes de prise en charge.