Rhumatologie
Gougerot-Sjögren : efficacité d’un anti-CD40, y compris dans les formes peu inflammatoires
Un antagoniste du CD40 ligand améliorerait nettement les symptômes du syndrome de Gougerot-Sjögren, y compris chez les patients peu inflammatoires mais très symptomatiques. Ces données de phase II ouvrent la voie à une prise en charge plus individualisée.

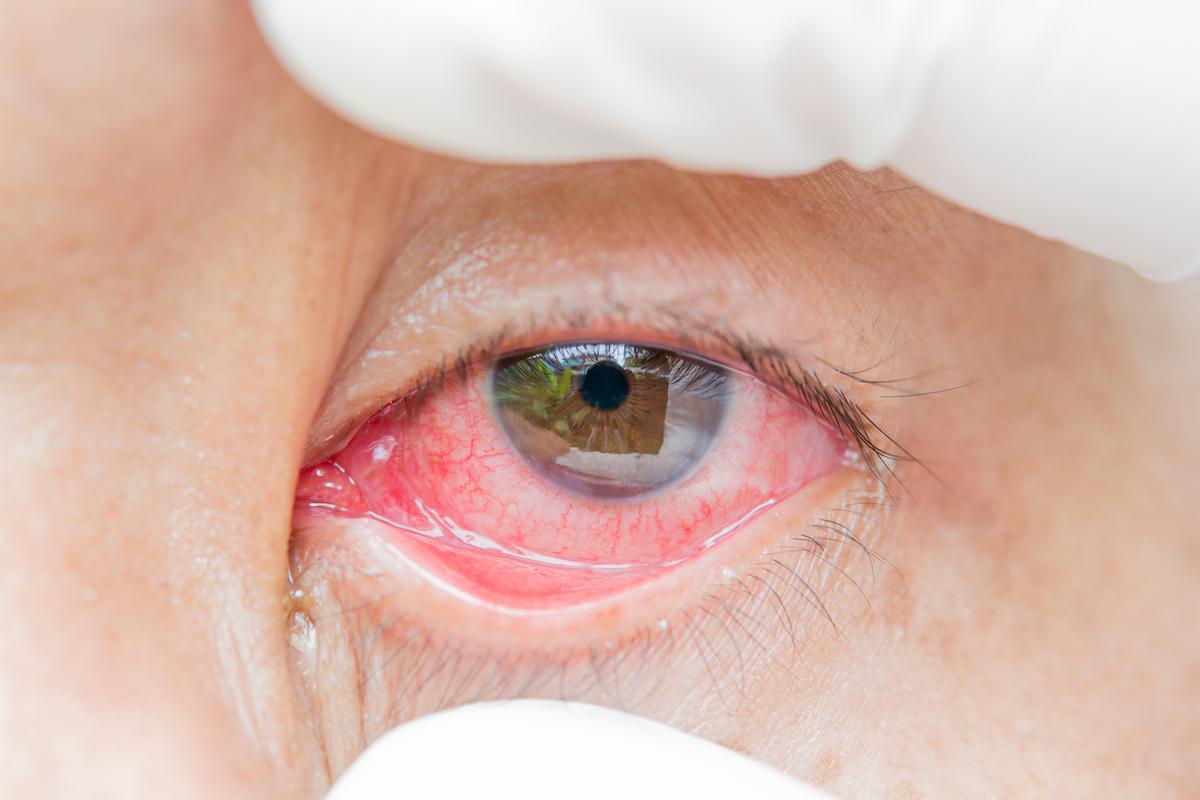
- Chepko/istock
Le syndrome de Gougerot-Sjögren (GS) demeure sans traitement de fond validé, alors que la fatigue, la sécheresse et les douleurs altèrent durablement la qualité de vie. Maladie auto-immune systémique caractérisée par une infiltration lymphocytaire des glandes exocrines, ce syndrome est caractérisé par le rôle crucial de l'axe de signalisation CD40/CD40L dans l'activation des cellules B, des cellules dendritiques et des cellules T, fortement impliquées dans la pathogénie. Le syndrome de Gougerot-Sjögren est actuellement dénué de traitement réellement efficace.
Le dazodalibep, une protéine de fusion non-anticorps, bloquant le CD40L, modulerait de façon large les interactions lymphocytes T/B, les cellules dendritiques et les cellules présentatrices d’antigènes. L’essai ALISS (phase II, randomisé, contrôlé, 2 étapes) a comparé le dazodalibep au placebo chez deux phénotypes : (i) malades « classiques » à activité systémique modérée – sévère (ESSDAI ≥ 5 ; n = 74) et (ii) patients « pauci-inflammatoires » (ESSDAI < 5) mais très symptomatiques (ESSPRI ≥ 5 ; n = 109). L’objectif principal de l’étape 1 était la variation d’ESSDAI ; à 24 semaines, la baisse moyenne versus placebo est de –2,2 points (p = 0,167), mais 61 % des patients sous dazodalibep obtiennent une réduction ≥ 5 points contre 35 % (p < 0,05). Dans l’étape 2 sur les patient peu inflammatoires, l’end-point principal était l’ESSPRI : le dazodalibep entraîne une diminution de –1,8 point versus –0,5 pour le placebo (différence –1,3 ; p = 0,0002) à la semaine 24, remplissant ainsi le critère de succès clinique.
Une efficacité objectivée dans 2 populations classiques de la maladie
Chez les patients à faible ESSDAI, l’amélioration fut homogène sur les trois domaines ESSPRI (sécheresse, fatigue et douleur) avec des réductions proches ou supérieures à 2 points, contre des modifications minimes sous placebo. Les échelles complémentaires de fatigue (FACIT-F) et de fardeau global confirment l’avantage du traitement. Dans la cohorte à activité plus élevée, l’effet sur la composante subjective n’apparait qu’en fin d’étude, tandis que des tendances positives non significatives (fatigue, fonction) confirment la logique d’une modulation CD40L.
En termes de tolérance, le profil est rassurant : effets indésirables émergents plus fréquents qu’avec le placebo (78 % vs 61 %), dominés par des infections des voies aériennes supérieures, un zona isolé et aucun événement indésirable grave lié au médicament. Aucun décès n’a été imputé au traitement ; aucune différence de tolérance n’est apparue entre les deux phénotypes.
Une méthodologie originale analysant plusieurs populations
ALISS adopte un design croisé original (24 semaines traitement, 16 semaines switch, 12 semaines off-drug) offrant une double lecture : validation sur une population standard de GS et, surtout, démonstration d’efficacité dans un sous-groupe souvent exclu des essais mais représentatif de la pratique clinique : les patients très symptomatiques malgré une faible activité inflammatoire objective.
La randomisation, le double-aveugle strict, l’évaluation combinée clinicien-patient (ESSDAI/ESSPRI) et le suivi prolongé post-traitement renforcent la robustesse de l’essai, bien que l’effectif reste modeste et essentiellement féminin (âge moyen ≈ 50 ans). Ces résultats suggèrent qu’un ciblage précoce de l’axe CD40/CD40L pourrait compléter ou remplacer des approches anti-B traditionnelles, particulièrement chez les sujets « pauci-inflammatoires » et hyperalgiques dont les plaintes demeurent insuffisamment prises en compte.
Selon les auteurs, le dazodalibep pourrait être proposé (après validation d’une phase III) aux patients souffrant d’une symptomatologie réfractaire, indépendamment de l’ESSDAI, afin de réduire la fatigue, la sécheresse et la douleur. Les futures études devront confirmer la durabilité du bénéfice, préciser les biomarqueurs prédictifs de réponse et évaluer l’impact sur les complications systémiques (pulmonaire, lymphomateuse).
Références :