Infectiologie
Covid-19 : le vaccin à ARN Pfizer-BioNTech serait protecteur à 90%
Selon des résultats intermédiaires, non publiés, de l’essai de phase 3, le vaccin à ARN contre la Covid-19, développé par les sociétés pharmaceutiques Pfizer et BioNTech, serait "efficace à 90%" en 2 doses chez les personnes non préalablement exposées au coronavirus.
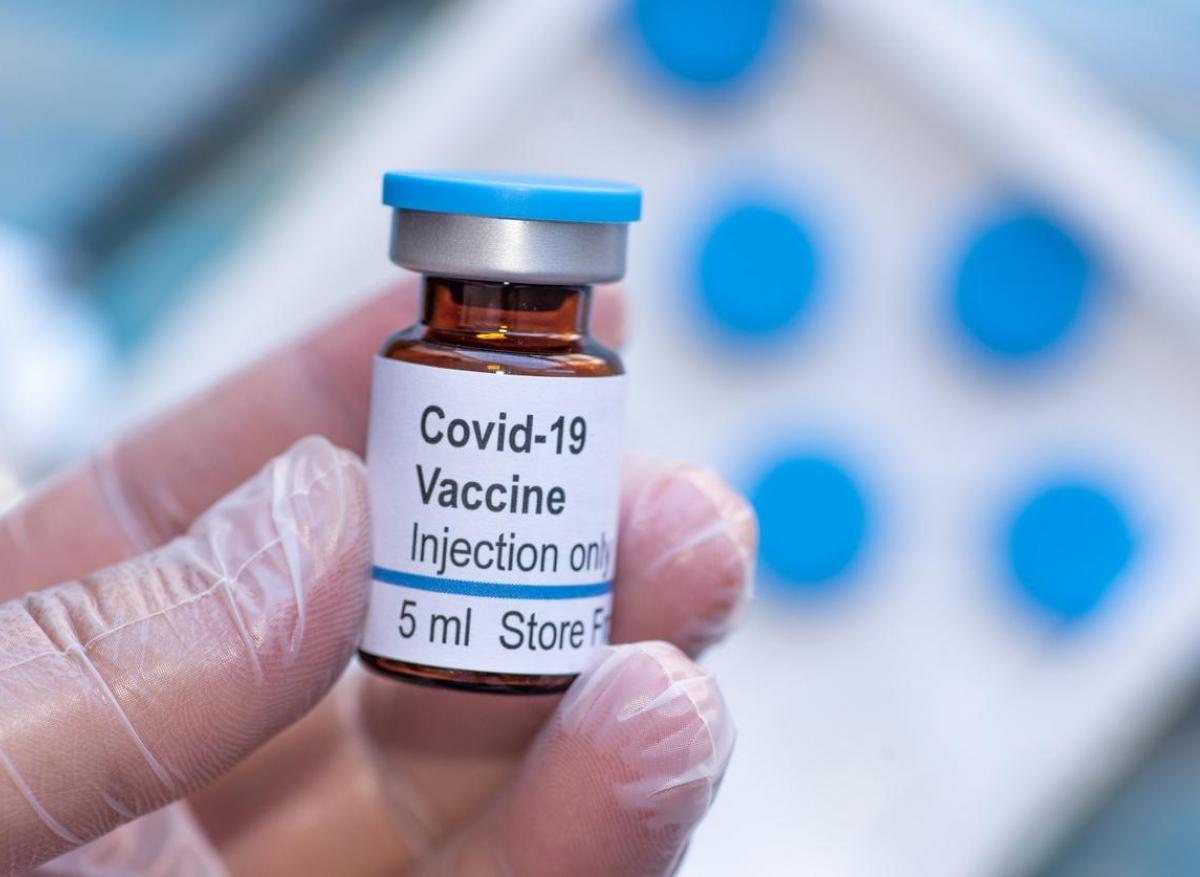
- Manjurul/iStock
Une nouvelle étape dans la lutte contre la pandémie de Covid-19. Alors que fin octobre, la Russie annonçait que son vaccin Spoutnik V entamait la phase finale des essais cliniques, ce seront peut-être les Américains qui dégaineront en premier leur vaccin. Ce lundi 9 novembre, la société pharmaceutique américaine Pfizer et son homologue allemande BioNTech ont annoncé avoir mis conjointement au point un vaccin à ARN "efficace à 90%". Ces résultats proviennent de la première analyse intermédiaire de leur essai de phase 3 encore en cours. Il s’agit de l’ultime phase des essais avant une demande d’homologation.
"Plus de huit mois après le début de la pire pandémie en plus d'un siècle, nous pensons que cette étape représente un pas en avant significatif pour le monde dans notre bataille contre la Covid-19", a déclaré le président-directeur général de Pfizer, Albert Bourla, dans un communiqué, ajoutant que "le premier ensemble de résultats de notre essai de vaccin Covid-19 de phase 3 fournit la preuve initiale de la capacité de notre vaccin à prévenir la Covid-19".
50 millions de doses disponibles d'ici fin 2020
Selon les résultats préliminaires communiqués par Pfizer et BioNTech (pas de publication), la protection des patients contre la Covid-19 a été obtenue sept jours après l'injection de la deuxième dose du vaccin et 28 jours après la première. Ce taux d’efficacité vaccinale "de plus de 90%" a été mesuré en comparant le nombre de participants infectés par le nouveau coronavirus dans le groupe qui a reçu le vaccin et dans celui sous placebo. Un niveau de protection qui n'était pas attendu par la plupart des spécialistes : ceux-ci se seraient contentés d'un peu plus de 50%
Des résultats encourageants donc pour cette étude sur 44 000 personnes, et qui pourraient permettre aux deux sociétés pharmaceutiques d’obtenir dans les prochains jours une utilisation d’autorisation d’urgence de leur vaccin aux États-Unis. Selon eux, les trois critères nécessaires (efficacité, absence de risque pour la santé et capacité de produire à grande échelle) seront remplis d'ici la fin du mois.
Vaccination des personnes prioritaires en vue
Si une telle autorisation d’urgence était accordée par l’agence américaine des médicaments (FDA), cela signifie que des membres du personnel hospitalier pourraient être les premiers à être vaccinés dans certains pays d’ici la fin de l’année, avance le Guardian. Les personnes à risques suivraient sans doute.
Pour leur vaccin Pfizer et BioNTech utilisent une technologie qui n'a jamais été approuvée pour une utilisation chez l'homme. Le vaccin est basé sur matériel génétique appelé ARN messager qui est injecté dans les cellules musculaires. Celles-ci se servent de l'ARN messager comme d'un code pour construire une protéine que l'on trouve à la surface du coronavirus. Les protéines sécrétées à partir de cet ARN codant stimulent alors le système immunitaire et sont censées conférer une protection durable contre le virus. D'autres entreprises, dont Moderna qui faisait jusqu'ici la course en tête, utilisent également la technologie de l'ARN messager.
La prudence reste de mise
La plupart des scientifiques indépendants mettent cependant en garde contre le risque de trop belle réussite des premiers résultats alors que c'est la première fois que l'on utilise un vaccin à ARN chez l'homme et avant qu'aucune donnée sur la sécurité et l'efficacité à long terme n'aient été revue par un comité de lecture et publiée. Le chiffre de 90% peut encore évoluer et personne ne sait combien de temps la protection de ce vaccin pourrait durer.
Néanmoins, ce développement fait de Pfizer la première entreprise à annoncer des résultats positifs au plan clinique pour un vaccin en phase finale, et propulse le duo Pfizer-BioNTech au premier rang d'une course mondiale effrénée qui a débuté seulement en février dernier et s'est donc déroulée à une vitesse record.
Un défi logistique
Selon Pfizer et BioNTech, jusqu’à 50 millions de doses de vaccins pourraient fournies dans le monde en 2020 et jusqu’à 1,3 milliard de doses en 2021.
La distribution à grande échelle de ce vaccin sera un défi logistique. Comme il est fabriqué avec de l'ARNm, les doses devront être conservées à des températures très basses. On ne sait pas encore comment les transporter en toute sécurité et comment les administrer à grande échelle, ni quel rôle le gouvernement jouera dans la vaccination. De plus, les personnes vaccinées devront revenir trois semaines plus tard pour recevoir une deuxième dose afin de compléter la vaccination.
À l’heure actuelle, aucun vaccin n'a encore reçu d'approbation pour une distribution commerciale à grande échelle. Selon l’Organisation mondiale de la Santé (OMS), 10 essais cliniques de vaccins sont actuellement en phase 3 dans le monde. Parmi eux, ceux de la biotech américaine Moderna, de plusieurs laboratoires chinois et du britannique AstraZeneca, en collaboration avec l'université d'Oxford.