Hématologie
LLC en rechute et/ou réfractaire : le zanubrutinib surclasse l’ibrutinib
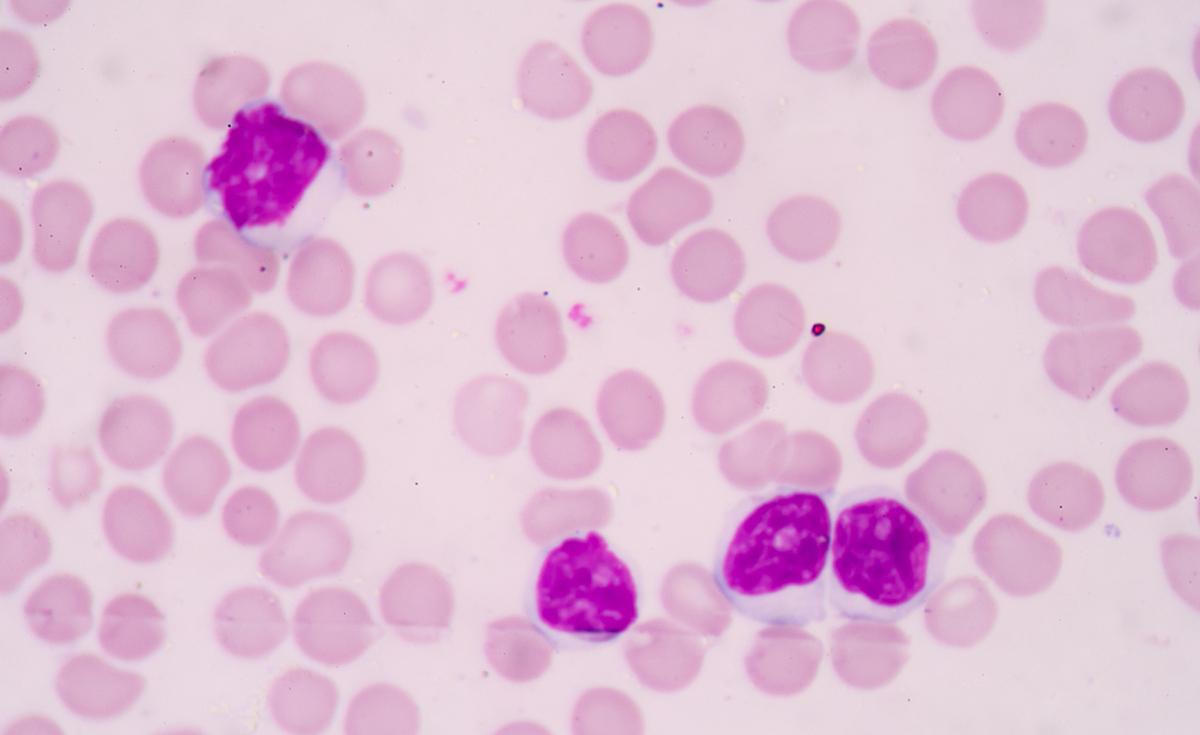
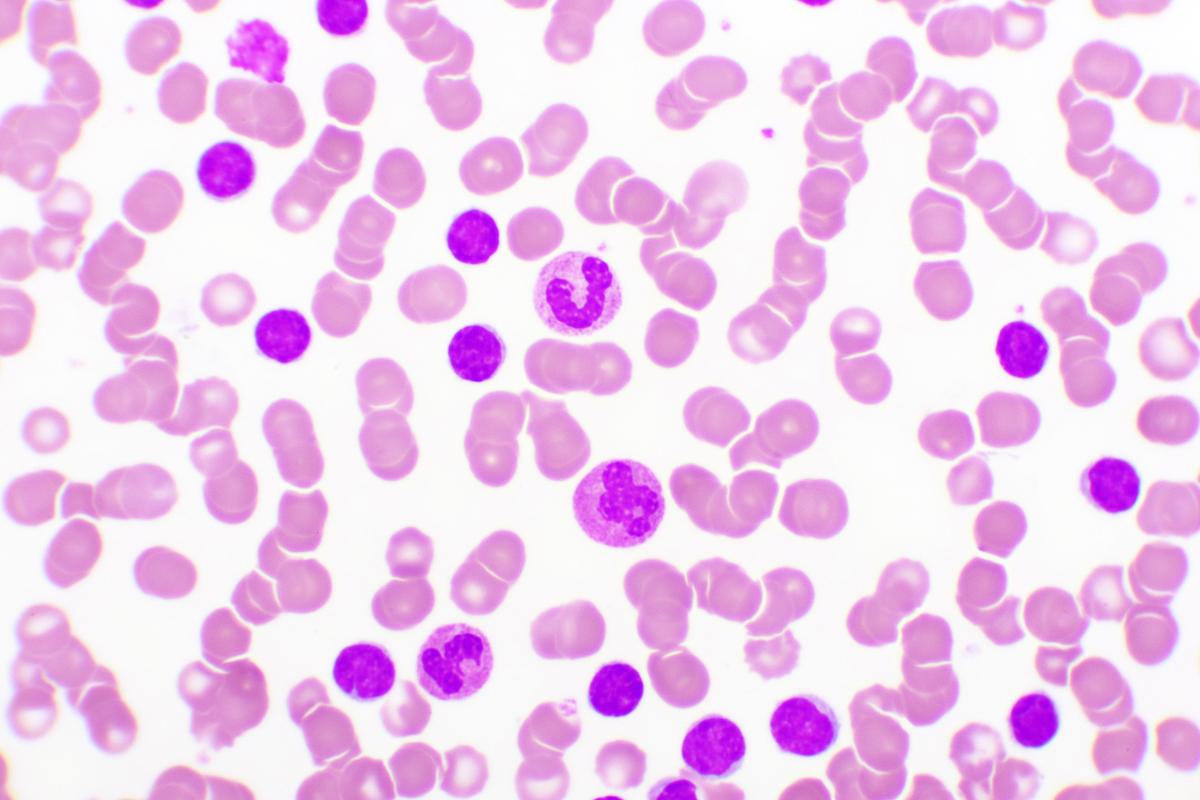
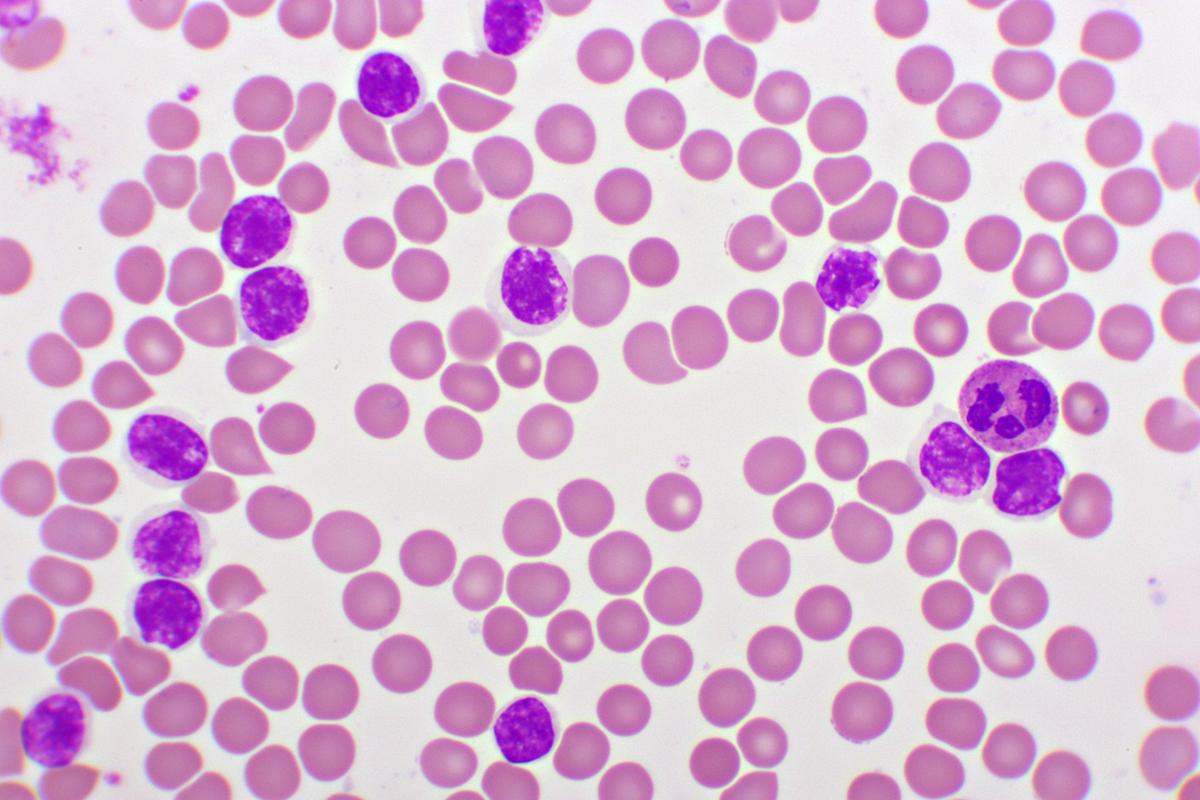
Les thérapies ciblées inhibant la tyrosine kinase de Bruton (BTK) ont révolutionné la prise en charge des patients atteints de leucémie lymphoïde chronique (LLC) ou de lymphome lymphocytique (LL). Cet article met en évidence la supériorité des inhibiteurs de BTK de 2ème génération chez les patients atteints de LLC/LL en rechute et/ou réfractaire.
- jarun011/istock
La LLC est la leucémie de l’adulte la plus prévalente dans le monde occidental 1. Bien que les progrès récents des thérapies ciblées aient transformé la prise en charge de cette hémopathie, la plupart des patients traités rechuteront et nécessiteront un traitement ultérieur.
L'ibrutinib, un inhibiteur de BTK de 1ère génération, est actuellement un standard de traitement en 1ère ligne et en situation de rechute et/ou réfractaire2. Cependant, son profil de tolérance (fibrillation atriale, hypertension artérielle, hémorragies) en limite l’utilisation et le développement d’inhibiteurs de nouvelle génération, plus spécifiques, laisse espérer un gain d’efficacité et une diminution des effets indésirables « off-target ».
Des essais cliniques de phases 2 et 3 ont précédemment démontré que le zanubrutinib, en raison d’une sélectivité supérieure à celle de l’ibrutinib, occupait complètement et durablement la cible (à la dose de 160 mg, administrée deux fois par jour) et permettait un gain significatif en termes de réponse globale3. Une étude a comparé le zanubrutinib à l’ibrutinib lors du traitement de patients atteints de LLC/LL en rechute et/ou réfractaire4.
Une population de LLC de haut-risque génétique
Entre novembre 2018 et décembre 2020, 652 patients atteints de LLC/LL ont été inclus et randomisés pour recevoir du zanubrutinib (n = 327) ou de l’ibrutinib (n = 325). L'âge médian était de 67 ans (35-90) et le nombre médian de lignes antérieures de traitement était de 1 (1-12).
Quarante-cinq pourcents des patients étaient considérés comme Bulky (volume tumoral ≥5 cm). Soixante-treize pourcents des patients présentaient un statut IGHV non-muté et 23% une anomalie de TP53 (délétion 17p et/ou mutation de TP53).
Une efficacité supérieure avec le zanubrutinib
Avec 29,6 mois de suivi médian, la survie sans-progression à 24 mois du groupe zanubrutinib est significativement supérieure à celle du groupe ibrutinib (respectivement 78,4% contre 65,9%, 95%CI 0,49 - 0,86 ; P = 0,002), y compris pour les patients qui ont une anomalie de TP53 (HR 0,53, 95%CI 0,31 - 0,88). Le bénéfice est observé pour tous les sous-groupes de patients : selon l'âge, le nombre de traitement antérieurs, selon le statut mutationnel IGHV.
A 24 mois de suivi, le pourcentage de patients sans échec thérapeutique est ainsi de 79,9% (95%CI, 75,1-83,9) dans le groupe zanubrutinib et de 65,0% (95%CI, 59,5 - 70,0) dans le groupe ibrutinib.
Moins d’événements indésirables cardiaques
Les principaux effets indésirables graves (≥3) dans les groupes zanubrutinib et ibrutinib sont la neutropénie (16,0% et 13,9%, respectivement) et l’hypertension artérielle (14,8% et 11,1%, respectivement).
Une incidence inférieure de troubles cardiaques est observée dans le groupe zanubrutinib (21,3%) en comparaison au groupe ibrutinib (29,6%), ayant engendré une interruption de traitement pour 1 patient (0,3%) du groupe zanubrutinib et 14 patients (4,3%) dans le groupe ibrutinib.
Au total, 69 patients (33 dans le groupe zanubrutinib, 36 dans le groupe ibrutinib) ont présenté un événement indésirable ayant entraîné le décès : dont 44 étaient des infections, principalement liées au Covid-19.
Conclusion
Le zanubrutinib, inhibiteur de BTK de nouvelle génération, est donc un traitement prometteur des patients atteints de LLC/LL en situation de rechute et/ou réfractaire.
Une efficacité supérieure à celle de l’ibrutinib et un profil de tolérance favorable, avec notamment la diminution des événements indésirables cardiaques, en font un vraisemblable standard de traitement dans ce contexte.
Références
- Siegel RL, Miller KD, Fuchs HE, Jemal A. Cancer statistics, 2022. CA Cancer J Clin 2022;72:7-33.
- Eichhorst B, Robak T, Montserrat E, et al. Chronic lymphocytic leukaemia: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2021;32:23-33.
- Hillmen P, Eichhorst B, Brown JR, et al. Zanubrutinib Versus Ibrutinib in Relapsed/Refractory Chronic Lymphocytic Leukemia and Small Lymphocytic Lymphoma: Interim Analysis of a Randomized Phase III Trial. J Clin Oncol 2023;41:1035-45.
- Brown JR, Eichhorst B, Hillmen P, et al. Zanubrutinib or Ibrutinib in Relapsed or Refractory Chronic Lymphocytic Leukemia. N Engl J Med 2023;388:319-32.