Rhumatologie
Neurofibromatose plexique inopérable : 1ère option crédible chez l’adulte NF1/PN
L’essai international randomisé KOMET de phase 3 démontre qu’un traitement continu par le selumetinib réduit significativement le volume des neurofibromes plexiformes inopérables et améliore la douleur chez des adultes porteurs d’une NF1, sans nouveau signal de toxicité ; ces résultats comblent un vide thérapeutique majeur jusque-là réservé à l’enfant.
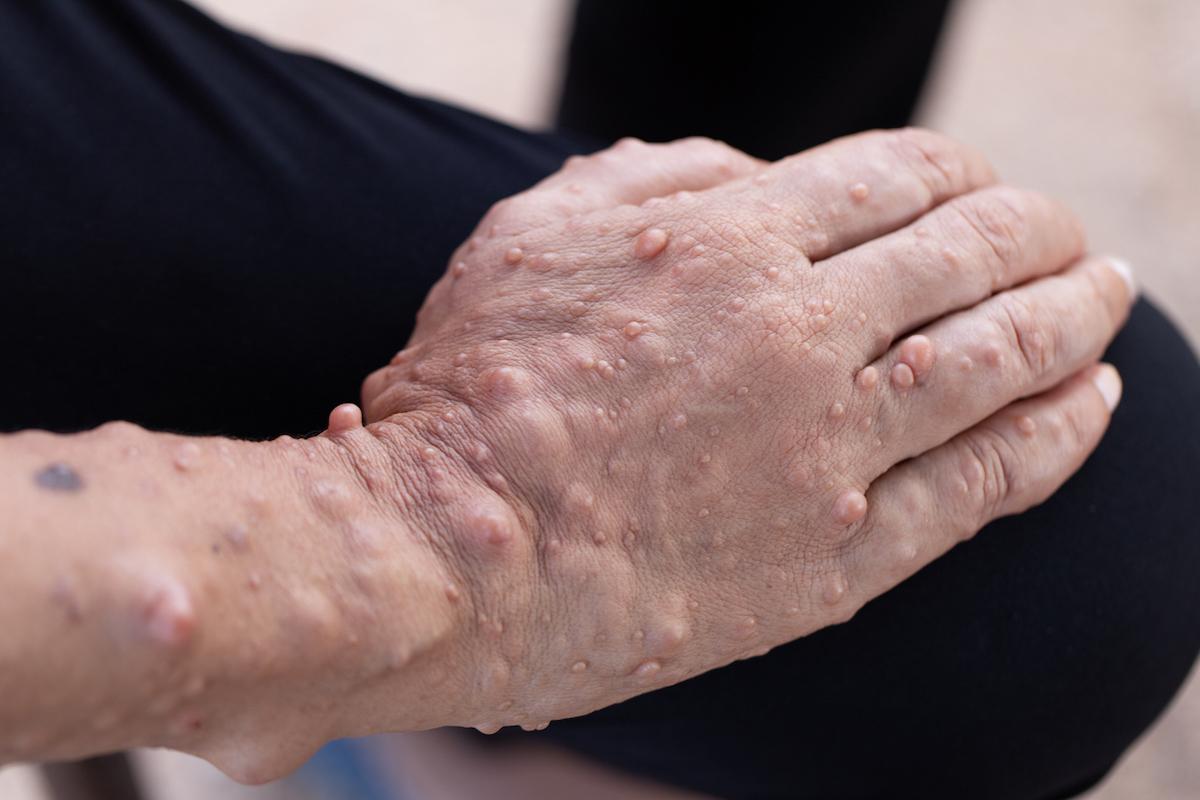
- Sinhyu/istock
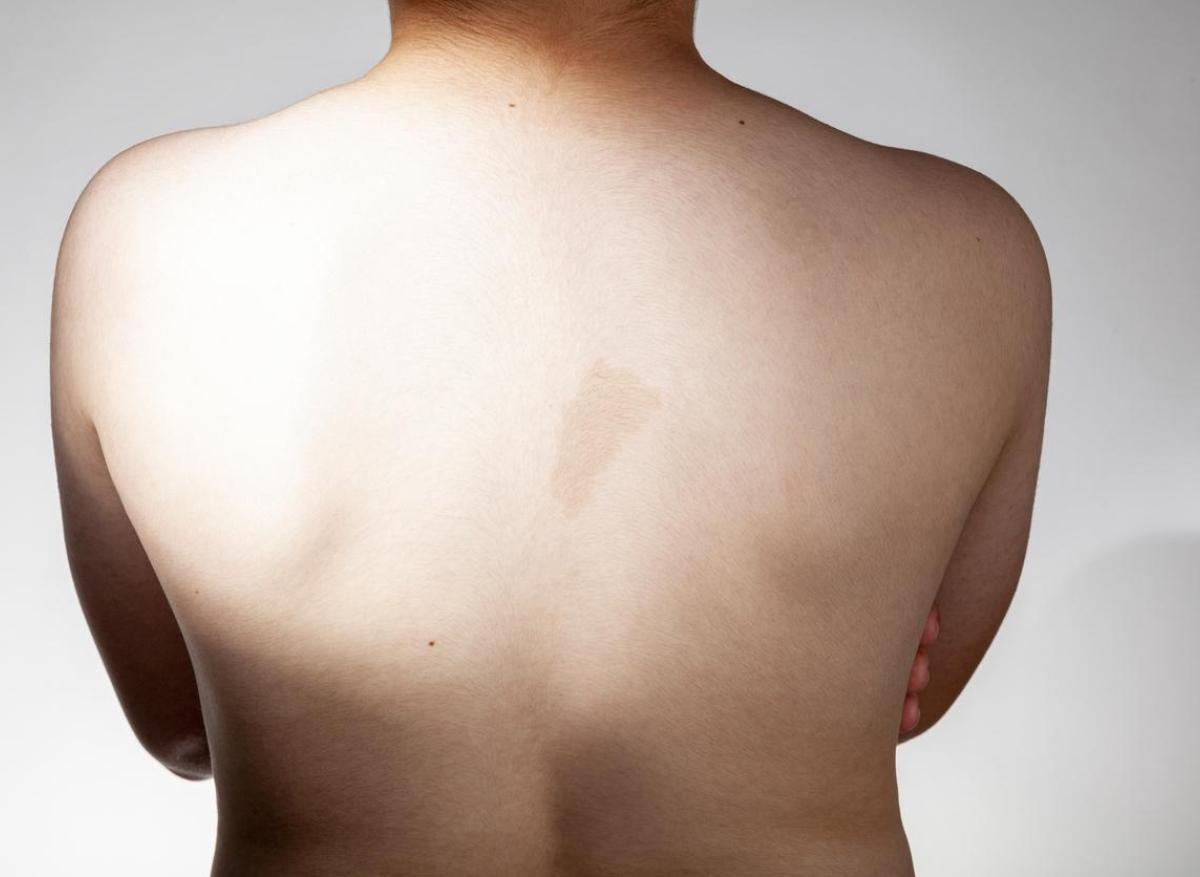
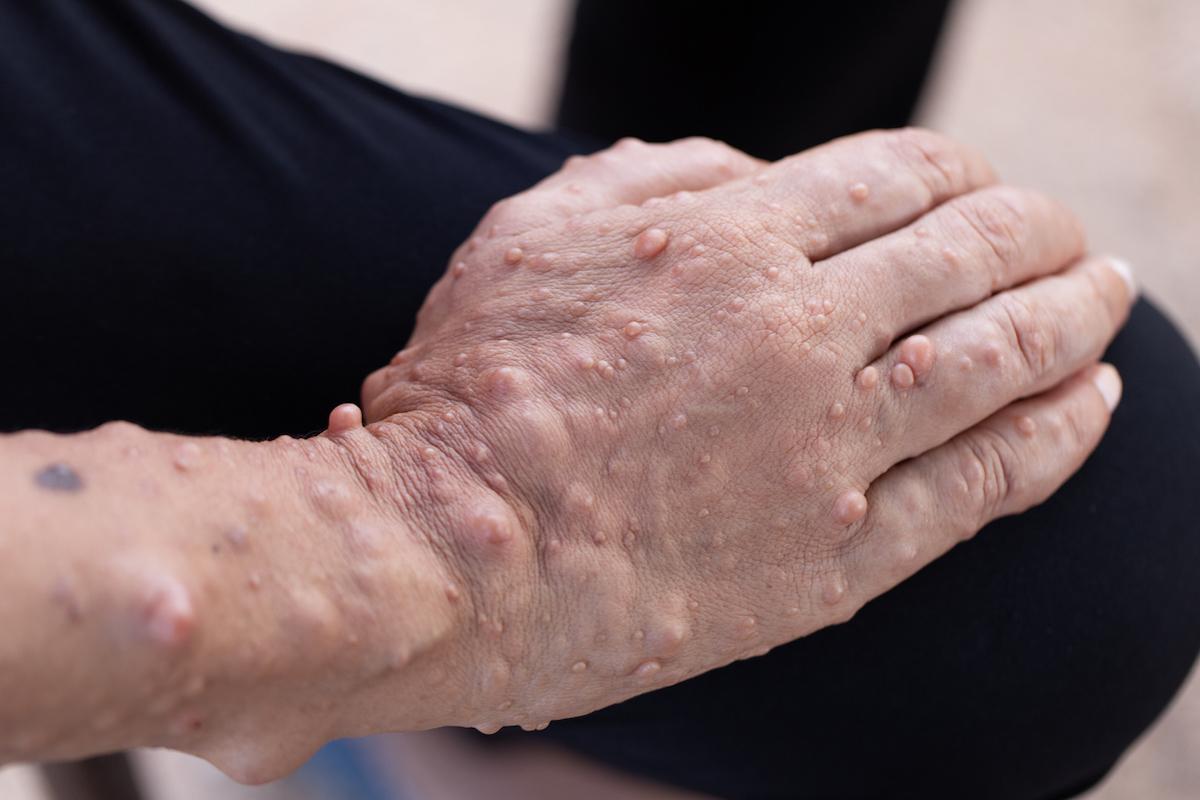
Au-delà des manifestations cutanées, la neurofibromatode de type 1 (NF1) touche 1 personne sur 2 500 et diminue l’espérance de vie de huit à quinze ans. La moitié des patients développent un ou plusieurs neurofibromes plexiformes, tumeurs nerveuses diffuses responsables de douleurs chroniques, de dysfonctions motrices et d’un risque de transformation sarcomateuse (MPNST ≈ 16 %). Faute d’exérèse complète réalisable, la prise en charge restait palliative chez l’adulte.
Une extension à l’adulte d’un inhibiteur des protéines kinases activées par les mitogènes 1 et 2
Après le succès pédiatrique du selumetinib, un inhibiteur puissant, sélectif et allostérique des protéines kinases activées par les mitogènes 1 et 2, (ORR 68 % dans SPRINT), KOMET a inclus 145 adultes NF1-PN symptomatiques, randomisés entre selumetinib ou placebo (cross-over autorisé à la progression).
Selon les résultats, présentés au congrès annuel de l’ASCO et publiés conjointement dans The Lancet, à l’analyse primaire (cycle 16, suivi médian 7,4 mois), le taux de réponse objective centralisée REiNS (Response Evaluation in Neurofibromatosis and Schwannomatosis) atteint 20 % sous selumetinib contre 5 % sous placebo (p = 0,011), avec un délai médian de réponse de 3,7 mois et une réduction volumique médiane de –28 % (vs –8 %).
Amélioration clinique et symptomatique avec tolérance correcte
Chez les sujets souffrant d’une douleur de base ≥ 3/10, la baisse moyenne du score NRS-11 à 12 mois est deux fois plus importante (-2,0 versus -1,3), s’accompagnant d’une diminution de l’analgésie systémique et d’une amélioration des domaines interférence-douleur (BPI). Les critères de qualité de vie PlexiQoL ne diffèrent pas encore entre groupes.
La tolérance, dominée par éruptions cutanées (27 %), troubles digestifs (24 %) et élévations CPK de grade 1-2, reste superposable au profil connu ; seules 6 % des patientes ont dû interrompre le traitement.
Une étude randomisée de bonne qualité
Ces données proviennent d’un protocole contrôlé, en double aveugle, mené sur 37 centres dans 12 pays. La taille d’échantillon (n = 145) confère une puissance statistique de 80 % pour détecter une différence absolue de 15 points de réponse ; la centralisation indépendante des images volumétriques garantit l’objectivité du critère principal. La randomisation 1 : 1 et la répartition équilibrée des facteurs pronostiques (âge médian 33 ans, douleur chronique 68 %, déformation 55 %) assurent la représentativité.
Les limites résident dans la courte durée du suivi pour apprécier la durabilité de la réponse, l’issue fonctionnelle et la prévention des tumeurs malignes de la gaine nerveuse périphérique (MPNST), objectifs des analyses finales (24 mois). Le schéma de cross-over pourrait atténuer ultérieurement l’effet global sur la qualité de vie.
La 1ère option non chirurgicale de la neurofibromatose de type 1
Selon les auteurs, le selumetinib devient la première option systémique validée chez l’adulte NF1-PN inopérable. L’instauration doit s’accompagner d’une surveillance dermatologique, ophtalmologique et biologique trimestrielle, l’arrêt temporaire ou la réduction de dose permettant de contrôler la majorité des effets indésirables.
À moyen terme, l’étude ouvre la voie à des stratégies combinées (analgésiques ciblés, immunothérapie) et à une utilisation préemptive dans les neurofibromatoses plexiformes à haut risque de transformation. L’enjeu de santé publique est conséquent : limiter la progression tumorale, la douleur et l’impact socio-professionnel chez ces jeunes adultes, tout en repoussant l’apparition des tumeurs malignes de la gaine nerveuse périphérique.
Les futures analyses pharmacogénétiques du réseau KOMET pourraient affiner la sélection des patients répondeurs et ajuster la posologie en fonction du métabolisme individuel, renforçant l’approche de médecine personnalisée dans la NF1. Une utilisation néoadjuvante de manière à réduire les mutilations associées à la chirurgie pourrait être envisagée à terme.