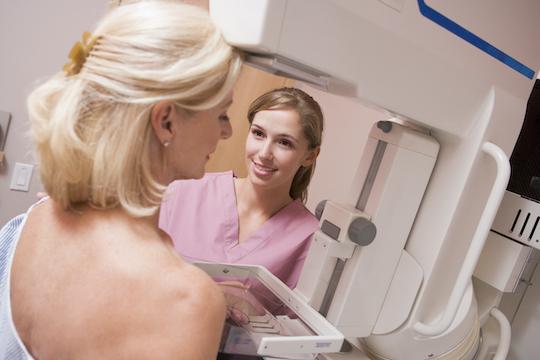
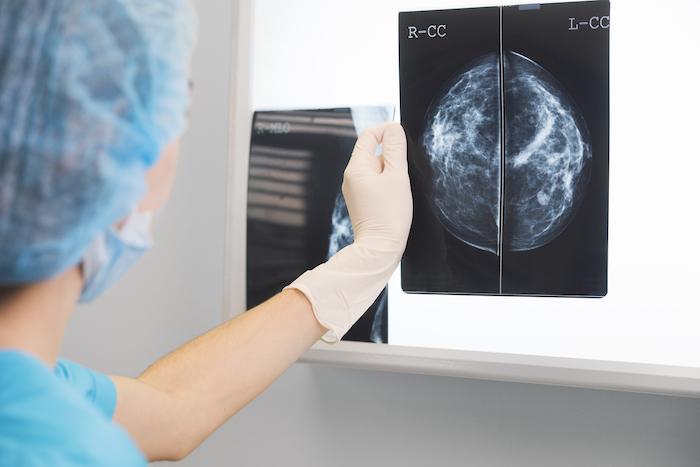
Onco-sein
Cancers du sein triple négatifs métastatiques : nouvel échec de l’immunothérapie
Récemment publiée dans le Lancet Oncol, l’étude de phase III, KEYNOTE 119, randomisant un traitement par pembrolizumab vs une chimiothérapie au choix de l’investigateur dans les cancers du sein triple négatifs métastatiques prétraités, n’a pas montré de bénéfice en survie globale.
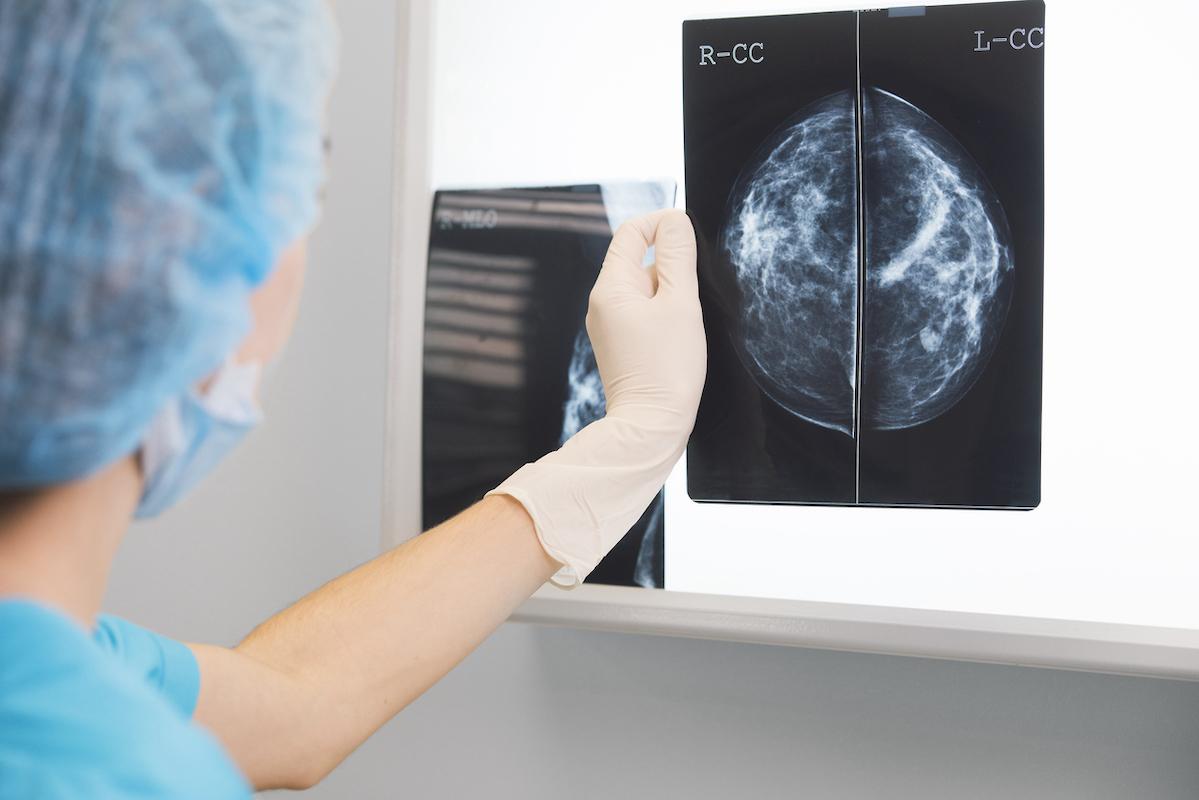
- thomasandreas/istock
Caractérisés par une agressivité tumorale et une mortalité élevée, les cancers du sein triple négatifs métastatiques ont malheureusement des perspectives thérapeutiques faibles avec des taux de réponse restant non satisfaisants (médiane de survie globale de 17 mois) et des toxicités liées aux traitements avérées, pour lesquels l’inclusion dans les essais cliniques est à privilégier.
Les études préliminaires de phase Ib et phase II, Keynote 012 et Keynote 086, avaient montré des résultats intéressants avec des taux de réponse objective de 18.5% et 5.3% respectivement pour les tumeurs PDL1+, et des survies globales à 12 mois de 43.1% et 39.8% respectivement.
Une étude randomisée sur 622 malades
L’étude Keynote 119, publiée par Winer dans The Lancet oncol, a évalué chez les patientes suivies pour un cancer du sein métastatique triple négatif déjà pré traité par au moins une ligne de chimiothérapie, un traitement par Pembrolizumab vs une chimiothérapie au choix de l’investigateur. Le résultat est net : elle ne montre pas de bénéfice concernant son critère de jugement principal, à savoir la survie globale, même chez les patientes PDL1+.
En pratique, de Novembre 2015 à Avril 2017, 622 patientes avec un cancer du sein métastatique triple négatif de novo ou après traitement néo/adjuvant, et déjà traitées par au moins une ligne de chimiothérapie en phase métastatique, à base de taxanes ou anthracyclines, sans dépasser 2 lignes de traitement systémique, ont été randomisées selon un schéma 1-1 : 312 dans le bras pembrolizumab à la dose de 200 mg toutes les 3 semaines, et 310 dans le bras chimiothérapie laissée au choix de l’investigateur (capecitabine, eribuline, gemcitabine ou vinorelbine).
Une population PDL1+
Les patientes étaient stratifiées selon le statut PDL1 : positif (≥1%) vs négatif (<1%), une antériorité de traitement néo/adjuvant vs métastatique de novo. La population, homogène dans les 2 groupes, a un âge médian de 52 ans, une antériorité de traitement néo/adjuvant pour 79% d’entre elles, et un score CPS ≥1 pour 65% des patientes dont 31% et 18% respectivement avec un score CPS ≥10% et ≥20%.
Le critère de jugement principal est la survie globale dans la population PDL1+ avec un score CPS ≥ 10, dans la population avec un score CPS ≥1, et dans la population en intention de traiter. Les critères de jugement secondaires étaient la survie sans progression, le taux de réponse objective, la durée de réponse, et la tolérance.
Pas de bénéfice en survie globale.
Avec un suivi médian de 31.4 mois dans le bras pembrolizumab et 31.5 mois dans le bras chimiothérapie, l’étude est négative concernant son critère de jugement principal : la médiane de survie globale des patientes avec score CPS ≥10% dans le bras pembrolizumab est de 12.7 mois vs 11.6 mois dans le bras chimiothérapie (HR = 0.78, 95% CI = 0.57–1.06, P = 0.057), et chez les patientes avec un score CPS ≥1% respectivement de 10.7 mois vs 10.2 mois (HR = 0.86, 95% CI = 0.69–1.06, P = 0.073). Enfin dans la population globale, la médiane de survie globale est de 9.9 mois dans le bras expérimental vs 10.8 mois dans le bras standard (HR = 0.97, 95% CI = 0.82–1.15).
Concernant les critères de jugement secondaire, le taux de réponse objective est similaire dans les 2 bras de traitement : chez les patientes avec un score CPS ≥ 10%, respectivement de 18% et 9%, chez les patientes avec un score CPS ≥1% de 12% et 9%, ainsi que la survie sans progression et la durée de réponse. Concernant la tolérance, 14% des patientes du bras pembrolizumab ont présenté des effets secondaires de grade 3-4 vs 36% dans le bras chimiothérapie, majoritairement d’ordre hématologique. 20% des patientes des 2 groupes ont présenté des effets secondaires jugés sévères, dont 1% dans les 2 groupes ayant conduit au décès.
Une tendance chez les patientes avec un score CPS élevé.
Des analyses exploratoires ont été réalisées chez les patientes présentant un score CPS≥20%, avec des résultats plus encourageants dans le bras pembrolizumab : une survie globale de 14.9 mois vs 12.5 mois dans le bras chimiothérapie, et un taux de réponse objective de 26% vs 12% respectivement.
Néanmoins ces résultats restent malgré tout décevants, et la place de l’immunothérapie dans les cancers du sein triple négatifs métastatiques tend difficilement à s’imposer notamment avec l’actualisation récente d’IMpassion 130. Il est probable que le manque de données concernant l’intérêt d’un biomarqueur prédictif de réponse joue en notre défaveur.